Em reações de oxirredução um reagente atua como oxidante, recebendo elétrons enquanto um segundo atua como redutor, fornecendo elétrons. Essas reações podem ser utilizadas para gerar corrente elétrica e estão associadas com uma diferença de potencial, ou energia potencial. Caso essa diferença de potencial exista a reação ocorrerá de forma espontânea, esse é o caso de células voltaicas, ou pilhas. Caso contrário é necessário fornecer energia para que a reação ocorra, nesse caso o processo é chamado de eletrólise.
A espontaneidade de uma reação redox depende da tendência de um dos reagentes receber elétrons em relação ao outro. Por exemplo se um reagente A tem uma maior tendência em receber elétrons, ou seja é um agente oxidante mais forte, que o reagente B, podemos prever uma reação redox onde A oxida o reagente B. Esse tipo de análise pode ser utilizada para determinar se uma reação redox ocorrerá espontaneamente ou não.
O potencial de uma semi-reação é utilizado para medir essa tendência das substâncias em serem oxidadas ou reduzidas, entretanto uma vez que essa grandeza é relativa ela deve ser medida em relação a um referencial. No caso dos potenciais de redução é, por convenção, utilizado o potencial do hidrogênio como referência, sendo este estabelecido como zero. Podemos escrever para o hidrogênio:
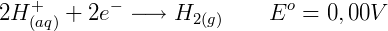
O eletrodo desenvolvido para produzir essa semi reação é o eletrodo padrão de hidrogênio (EPH). Outras semirreações tem seus potenciais avaliados em relação ao EPH. Por exemplo:
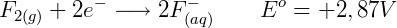
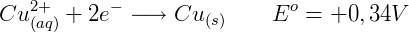
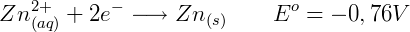
Onde um valor positivo indica que a semi-reação é favorável em relação à referência. Por exemplo a redução do flúor (F) tem uma energia E = +2,87 V em relação à hidrogênio (H), logo o flúor é capaz de oxidar hidrogênio molecular para formar fluoreto e íons de hidrogênio. A reação completa será:
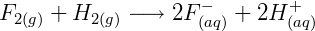
Podemos fazer uma análise semelhante para qualquer par de reagentes. Para isso basta calcular a diferença de potencial da reação entre eles utilizando o potencial de redução padrão:
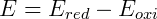
Onde Ered é o potencial padrão de redução da espécie sendo reduzida e Eoxi é o potencial padrão de redução da espécie sendo oxidada. Por exemplo, o potencial de uma reação onde o cobre é reduzido e o zinco é oxidado é:
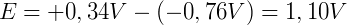
O valor positivo indica que essa reação ocorre espontaneamente.
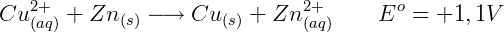
Observe que se invertermos o agente redutor e oxidante o sinal do potencial muda. Nesse caso, se o zinco fosse o agente oxidante o potencial seria -1,10 V indicando que a reação não ocorre espontaneamente.
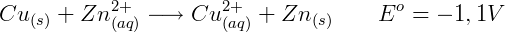
Nos links abaixo você encontrará tabelas com o potencial de redução de diversas substâncias:
http://www.chemeddl.org/services/moodle/media/QBank/GenChem/Tables/EStandardTable.htm
http://hyperphysics.phy-astr.gsu.edu/hbase/Tables/electpot.html
Referência:
BROWN, Theodore; LEMAY, H. Eugene; BURSTEN, Bruce E. Química: a ciência central. 9 ed. Prentice-Hall, 2005.
Texto originalmente publicado em https://www.infoescola.com/eletroquimica/potencial-de-reducao/