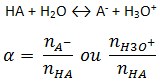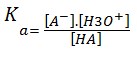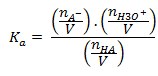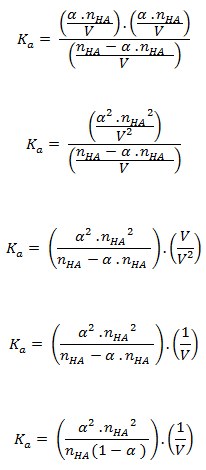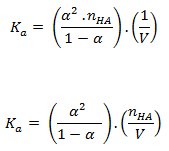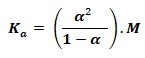O grau de ionização de um ácido indica a porcentagem ou fração molar de íons H3O+ formados pela liberação de íons H+ de um ácido de Arrhenius ou do ânion correspondente em relação à quantidade inicialmente adicionada. Dessa forma, se 1 mol de ácido monoprótico HA é diluído em água líquida pura e, desta quantidade de matéria, 0,05 mol ioniza-se completamente, pode-se afirmar que o grau de ionização será de 5% ou α = 0,05. Portanto, 95% do ácido (0,95 mol) permanecerá na forma molecular:
A constante de ionização de um ácido leva em consideração a concentração das espécies envolvidas e não apenas a quantidade de matéria. Para essa reação:
Vale ressaltar que a concentração de H2O já está embutida no valor de Ka, que, por ser um solvente cuja concentração é extremamente alta (até porque as concentrações de H3O+ e OH- são da ordem de 10-7 M), não faz parte do denominador da equação da constante.
Outro ponto a ser observado é que a concentração de HA não será a mesma que a inicial, pois uma parte sofreu ionização. Assim, deve-se “descontar” o número de mols de ânion ou íons hidroxônio do total.
A lei da diluição de Ostwald é, justamente, descrita como a relação matemática entre o grau de ionização α (em fração molar) e a constante de equilíbrio Ka.
Da definição de concentração vem:
Da definição de grau de ionização vem:
Considerando-se o “desconto” no número de mols de HA (inicialmente igual a nHA e agora igual a nHA - α . nHA) e substituindo na fórmula de Ka:
E, como nHA/V = concentração inicial M do ácido, finalmente tem-se:
Se o ácido possuir grau de ionização muito pequeno, o valor 1-α pode ser aproximado para 1, assim:
É importante lembrar que essa relação só pode ser usada em reações de ionização de ácidos monopróticos (com um átomo de hidrogênio ionizável) ou polipróticos considerando apenas uma ionização por vez (pois os valores de α e M mudarão com cada dissociação).
Texto originalmente publicado em https://www.infoescola.com/fisico-quimica/lei-da-diluicao-de-ostwald/