Os compostos químicos podem ser representados de diversas formas, no entanto cada um tem sua estrutura diferenciada, pois depende de quantos elétrons possuem na camada de valência, entre outras particularidades. Dentre diversas maneiras de representar uma molécula existe a fórmula estrutural apresentada a seguir.
Conteúdo deste artigo
Fórmula Estrutural
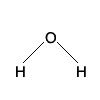
Esse é o tipo de apresentação detalhada de como os átomos de uma molécula estão ligados entre si. Por exemplo, a molécula de água, onde dois átomos de Hidrogênio se unem a um átomo de Oxigênio.
Na fórmula estrutural além de fornecer o número de átomos ligados, pode observar também como eles estão ligados entre si.
Tipos de fórmula estrutural
Fórmula Condensada
Nesse tipo de fórmula as ligações entre os átomos não são representadas. Exemplo de fórmula condensada:
Hexano: (C6H14)
CH3 CH2 CH2 CH2 CH2 CH3
No entanto, se algum índice se repetir deve-se colocá-lo entre colchetes e indicar quantas vezes ele aparece na fórmula:
CH3 [CH2]4 CH3
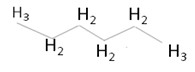
Fórmula Condensada Linear
Os carbonos são representados em forma de linhas em ziguezague. Cada extremidade da linha há um carbono. Como o carbono faz quatro ligações o restante é hidrogênio. Exemplo: Na ponta e no fim da reta, o carbono está fazendo três ligações então há três hidrogênios. No fim e início de cada reta o carbono está fazendo duas ligações por isso tem dois hidrogênios.
 Fórmula eletrônica ou de Lewis
Fórmula eletrônica ou de Lewis
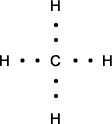
Esta fórmula apresenta os elétrons da camada de valência por pontos, e o elemento químico no centro. Exemplo: molécula do gás metano:
 Fórmula de Couper
Fórmula de Couper
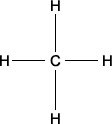
Neste tipo de fórmula retira-se os pontos e representa-se os elétrons da camada de valência por traços. Exemplo: outra forma de representar a molécula do gás metano.
Para escolher a fórmula estrutural adequada, deve levar em consideração os detalhes que deseja apresentar, pois algumas formas são simples porém outras mais complexas.
Bibliografia:
BARBOSA, Luis Cláudio de Almeida, Introdução á Química Orgânica. São Paulo,UFV,2004. pg, 11-12
Texto originalmente publicado em https://www.infoescola.com/quimica/formula-estrutural/