Uma substância simples é aquela que apresenta apenas um elemento químico, como por exemplo, o gás oxigênio O2. Quando uma substância simples varia o número de átomos, ou sua estrutura cristalina, outra substância é formada e a este fenômeno atribuímos o nome de Alotropia. Em síntese a Alotropia ocorre quando um elemento químico forma duas ou mais substâncias simples diferentes.
Quando tratamos de formas alotrópicas obtidas a partir da variação na atomicidade devemos lembrar do gás oxigênio e do gás ozônio. Suas fórmulas são O2 e O3 respectivamente, havendo a variação de um átomo de oxigênio entre eles. Esta variação lhes confere propriedades diferentes e ao mesmo tempo essenciais para o funcionamento da vida na Terra, pois o gás oxigênio é necessário para a respiração e o gás ozônio é um dos responsáveis pela proteção contra os raios ultravioleta sendo encontrado na camada que inclusive leva o seu nome, a camada de ozônio.
O enxofre é um elemento que possui variações alotrópicas, as principais são: enxofre ortorrômbico, ou apenas rômbico e enxofre monoclínico. As estruturas das moléculas ocorrem em forma de anel com oito átomos de enxofre (S8), porém possuem arranjos diferentes entre si originando assim diferentes cristais. O enxofre rômbico e o monoclínico são encontrados em regiões vulcânicas e utilizados para obtenção de ácido sulfúrico (H2SO4) industrialmente, bem como fazem parte da composição de fertilizantes.

Diamante. Foto: everything possible / Shutterstock.com

Grafite. Foto: Fablok / Shutterstock.com
O fósforo pode apresentar diversas formas alotrópicas. As mais conhecidas o fósforo vermelho e o fósforo branco sendo o último extremamente reativo e consequentemente instável. Possuem fórmula molecular P4 variando apenas sua estrutura e são utilizados em artigos de pirotecnia além de aditivos de óleos industriais.
Outro exemplo que ilustra bem a formação de alótropos devido a variação da estrutura são as formas alotrópicas do carbono: grafite e diamante. O grafite possui uma estrutura em forma de lâminas e o diamante possui uma estrutura mais compacta o que confere a ele uma maior estabilidade. O diamante é o mineral com maior dureza conhecido e devido a isso é utilizado inclusive como broca para perfuração, além é claro da sua comercialização como pedra preciosa. O grafite é facilmente desgastável por isso é utilizado em lápis além é claro da utilização em peças refratárias e lubrificantes. Outra forma alotrópica do carbono é o fulereno que é muito utilizado pela medicina como antiviral, antioxidante e antimicrobiano.
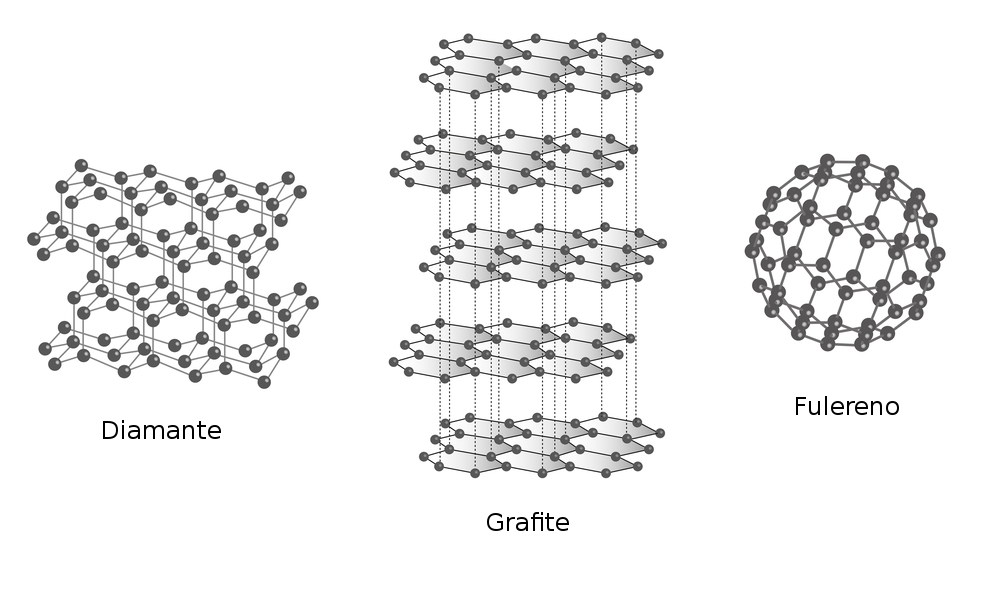
Formas alotrópicas do carbono. Ilustração: magnetix / Shutterstock.com
Atualmente tem se desenvolvido muito a pesquisa na área da Nanociência relacionada aos nanotubos, que são estruturas de carbono em forma de “rolo” ou tubo extremamente pequenas. Esses nanotubos possuem grandeza na escala de 10-9 a 10-12 metros e são obtidos através de folhas de grafite enroladas quimicamente. Esses materiais são largamente utilizados em circuitos eletrônicos e são muito estáveis, resistentes e conduzem bem corrente elétrica. Desta forma são de extrema importância para o desenvolvimento tecnológico em geral.
Fontes:
FELTRE, R. Química Geral. Vol 1. 6ª edição. Editora Moderna: São Paulo, 2004.
http://www.tecmundo.com.br/nanotecnologia/2640-o-que-sao-nanotubos-de-carbono-.htm
Texto originalmente publicado em https://www.infoescola.com/quimica/alotropia/