As substâncias puras (que só possuem um único componente) podem ser divididas em simples e compostas.
Substância pura simples
É formada por apenas um tipo de elemento, sob a forma de íons iguais.
Exemplos: H2 (Gás Hidrogênio), N2 (gás nitrogênio), O2 (gás oxigênio).
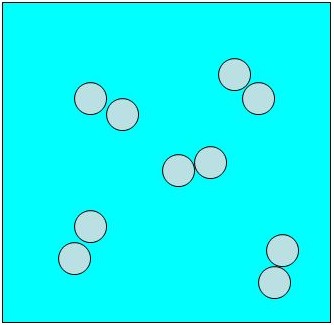
Representação com átomos simbolizados por bolinhas para a molécula de H2.
Em alguns casos, um mesmo elemento pode formar substâncias simples diferentes dependendo da maneira como ele se combina, formando alótropos. Esse é o caso do oxigênio, que forma o O2 (gás oxigênio) e o O3 (gás ozônio).
Muitos elementos da Tabela Periódica existem como substância pura. A maior parte da Tabela forma substâncias puras no estado físico sólido (no caso dos metais, por exemplo) e gasoso (no caso o gás oxigênio, por exemplo). As duas únicas substâncias puras simples líquidas são o mercúrio e o bromo.
As substâncias simples podem ser classificadas em monoatômicas, diatômicas, triatômicas, etc. como vemos a seguir:
- Monoatômicas: é o caso dos gases nobres, que existem de maneira isolada na natureza, como o gás hélio (He), o gás argônio (Ar) e também dos metais como o ferro (Fe) e o alumínio (Al).
- Diatômicas: é o caso do oxigênio (O2) e do hidrogênio (H2) do ar.
- Triatômicas: o gás ozônio (O3) é formado por três átomos de oxigênio como já mencionado no texto.
Substância pura composta
Pode ser formada por mais de um tipo de elemento, sob a forma de íons diferentes. Não existe limite para o número de átomos que formam uma substância composta.
Exemplos: CO2 (dióxido de carbono), NaCl (cloreto de sódio), H2O (água).
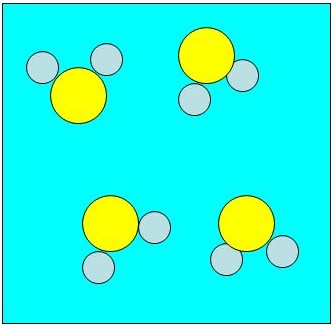
Representação com átomos simbolizados por bolinhas para a molécula de H2O.
Assim como nas substâncias puras, nas compostas também há a possibilidade de dois elementos formarem, dependendo da proporção entre eles, substâncias diferentes. Neste caso não chamados de alotropia pois é apenas uma combinação diferente de átomos. Mas é preciso levar em conta que para ser substância pura, a composição não pode variar.
Exemplo: H2O (água) e H2O2 (água oxigenada).
Note que ambas as substâncias possuem hidrogênio e oxigênio, mas não são a mesma.
Uma particularidade de algumas substâncias compostas é a capacidade de serem decompostas em substâncias simples. A água (H2O), por exemplo, pode ser decomposta em gás oxigênio e gás hidrogênio por eletrólise, assim como cloreto de sódio (NaCl) que, no seu estado fundido, ao passarmos uma corrente elétrica, sofre uma reação de oxirredução que dará origem a duas substâncias simples, o sódio metálico (Na) e o gás cloro (Cl2).
Bibliografia:
Atkins, P.W., Jones, L., Princípios de química: questionando a vida moderna e o meio ambiente 5ª ed., Porto Alegre: Ed. Bookman, 2012.
Usberco J., Salvador E., Química Geral, 12ª.ed., São Paulo: Saraiva, 2006.
http://www2.eesc.usp.br/netef/Oscar/Aula4t.pdf
Texto originalmente publicado em https://www.infoescola.com/quimica/substancias-simples-e-compostas/