Substância pura é toda substância formada por apenas um tipo de molécula, de composição química invariável e homogênea, e que tenha propriedades físicas e químicas constantes. A substância pura pode existir em mais de uma fase, porém, nesses casos, a composição das fases será a mesma.
Em suma, substância pura é todo material com as seguintes características:
- Unidades estruturais (moléculas, conjuntos iônicos) quimicamente iguais entre si.
- Composição fixa, do que decorrem propriedades fixas, como densidade, ponto de fusão e de ebulição, etc.
- A temperatura se mantém inalterada desde o início até o fim de todas as suas mudanças de estado físico (fusão, ebulição, solidificação, etc.).
O gráfico de aquecimento da água pura está representado abaixo:
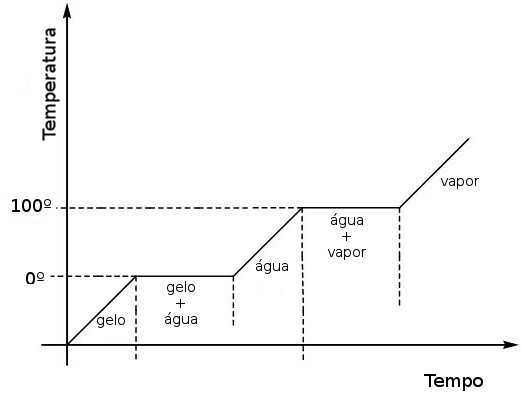
No gráfico observa-se que o gelo, ao derreter, muda de estado físico (fusão) e esse processo acontece na temperatura constante de 0 ºC. Depois, ao atingir a temperatura de 100 ºC, a água líquida começa a passar para o estado vapor (ebulição) e esse processo também ocorre sem mudança de temperatura.
As substâncias puras podem ser divididas em simples e compostas.
Conteúdo deste artigo
Substância pura simples
É formada por apenas um tipo de elemento.
Exemplos:
- H2 (gás hidrogênio)
- N2 (gás nitrogênio)
- O2 (gás oxigênio)
Substância pura composta
Pode ser formada por mais de um tipo de elemento.
Exemplos:
- CO2 (dióxido de carbono)
- NaCl (cloreto de sódio)
- H2O (água)
As substâncias puras podem se apresentar em forma de sistema homogêneo ou heterogêneo:
Sistema homogêneo
Se apresenta em apenas uma fase, ou seja, vemos somente uma coisa dentro do frasco. Na foto abaixo vemos a substância pura água no estado líquido.

Água pura. Foto: Edler von Rabenstein / Shutterstock.com
Sistema heterogêneo
Apresenta mais de uma fase, ou seja, observamos mais de uma coisa dentro do frasco. Na foto abaixo vemos a substância pura água no estado líquido e também no estado sólido (gelo), no entanto, ambas as representações são água.

Sistema heterogêneo. Foto: Melica / Shutterstock.com
É importante tomar cuidado com situações onde lidamos com uma mistura que se comporta visualmente como substância simples. O sangue por exemplo, pode parecer uma substância simples, mas é uma mistura de diversos componentes (água, hemácias, plasma, etc). A água do mar é uma mistura de água com sais dissolvidos. Outros exemplos são o leite, a maionese, a madeira, entre outros.
O ar que respiramos também é um exemplo de mistura que aparentemente parece substância pura e é composto por: gás nitrogênio (N2) = 78%, gás oxigênio (O2) = 21%, gás argônio (Ar) = 1% e gás carbônico (CO2) = 0,03%. O resto da composição são impurezas e partículas sólidas dissipadas.
Bibliografia:
Atkins, P.W., Jones, L., Princípios de química: questionando a vida moderna e o meio ambiente 5ª ed., Porto Alegre: Ed. Bookman, 2012.
Usberco J., Salvador E., Química Geral, 12ª.ed., São Paulo: Saraiva, 2006.
http://www2.eesc.usp.br/netef/Oscar/Aula4t.pdf
Texto originalmente publicado em https://www.infoescola.com/quimica/substancia-pura/