O modelo dos gases ideais, ou perfeitos, é uma ferramenta muito útil em diversos ramos da ciência. Embora nenhum gás seja de fato ideal, a maioria deles tem uma faixa de condições onde seu comportamento é bem descrito pelo modelo. A equação de estado de um gás ideal é escrita da seguinte forma:
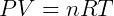
P = pressão, V = volume, n = quantidade de gás, R = constante dos gases perfeitos, T = temperatura
É possível notar que não há nessa equação quaisquer considerações sobre a natureza química do gás. No entanto percebemos empiricamente que os gases se comportam de formas distintas, especialmente quando submetidos à condições extremas, de alta pressão por exemplo. Modelos para gases reais, que levem em consideração a composição dos mesmos são, portanto, necessários.
As duas principais suposições do modelo de gases ideais são os seguintes:
- O volume da partícula/molécula é desprezível;
- Não existem interações entre as partículas/moléculas.
Com isso em mente, em 1873 o holandês Johannes Diderik van der Waals trabalhou para encontrar uma descrição física para a não idealidade dos gases. Embora o atomismo ainda não fosse amplamente aceito na comunidade científica, van der Waals acreditou que interações entre as partículas constituintes do gás e o volume não desprezível destas seria responsável pelos desvios de comportamento de alguns gases.
Primeiramente consideramos que nem todo volume do recipiente está disponível para o gás ocupar, uma vez as partículas nele tem um volume finito. Podemos utilizar um volume efetivo definido como:
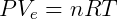
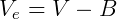
Onde V é o volume do recipiente e B é o volume total ocupado pelas partículas. É conveniente expressão o volume total B em função do número de mols de gás no sistema, logo:
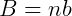
Onde b é o volume molar das partículas/moléculas do gás. Temos então:
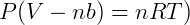
A segunda consideração diz respeito à atração entre as partículas do gás. Essas forças de atração seriam praticamente nulas no seio da mistura, porém próximo à fronteira as partículas sentiriam uma força em direção ao centro que reduziria a intensidade dos impactos nas paredes do recipiente. Van der Waals considerou que essa atração seria proporcional ao quadrado da concentração do gás.
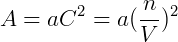
A pressão deve então ser reduzida por esse fator:
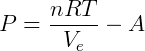
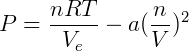
Colocando as duas correções juntas obtemos:
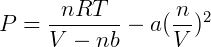
ou
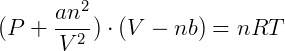
Que é a equação de estado de van der Waals, onde as constantes a e b são parâmetros experimentais que dependem da natureza do gás.
Apesar de existirem hoje diversas equações de estado, a formulação de van der Waals é particularmente importante porque atribui sentido físico às correções, além disso ajustando sua equação a dados experimentais é possível obter informações sobre o gás. A constante b por exemplo é uma estimativa do volume das moléculas ou átomos que constituem o gás.
As ideias de van der Waals a respeito da interação de moléculas lhe rendeu grande destaque em ciências moleculares, como a química, ele foi o primeiro cientista a estabelecer esses conceitos de forma satisfatória. Hoje chamamos de forças de van der Waals as forças intermoleculares responsáveis por inúmeros fenômenos do dia a dia.
Texto originalmente publicado em https://www.infoescola.com/fisica/equacao-de-van-der-waals/