A calorimetria é o ramo da física que estuda o calor. O objetivo da calorimetria não é apenas entender o conceito de calor, mas também calcular sua quantidade. Antes de saber como se calcula a quantidade de calor, vamos esclarecer alguns conceitos importantes.
O calor é energia térmica transferida de um corpo com maior temperatura para outro de menor temperatura. Nenhum corpo possui calor, ele é apenas a energia em trânsito de um corpo para o outro. Terminada a transferência, já não há mais calor, pois neste caso atingiu-se o equilíbrio térmico (corpos a mesma temperatura).
Existem dois tipos de calor: o calor sensível (ou específico) e o calor latente. O calor sensível é aquele que apenas é suficiente para variar a temperatura do corpo, não ocorrendo uma mudança de estado. Seu cálculo será visto adiante (pela equação fundamental da calorimetria). Já o calor latente é aquele que provoca mudança de estado no corpo, mas não faz a sua temperatura variar. Ele é determinado pela equação:
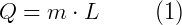
em que m é a massa, L é o calor latente da substância e Q é a quantidade de calor necessária para uma mudança de estado físico, sem variação de temperatura.
Existe uma característica que é inerente do corpo que transmitirá ou receberá o calor, pois não basta que o calor seja transferido, é necessário que um corpo esteja apto a ceder ou receber este calor. Esta característica chama-se Capacidade térmica. Ela mede o quanto que uma substância pode reter de calor e por quanto tempo pode mantê-lo.
Por ser uma característica de cada corpo, as substâncias possuem diferentes capacidades térmicas. Um exemplo é a areia da praia e a água do mar. A areia esquenta muito rápido, mas esfria rapidamente também, enquanto que a água demora para esquentar, contudo esfria mais devagar da mesma forma. Neste caso, a água possui capacidade térmica maior que a areia.
A capacidade térmica (C) também é definida como a quantidade de calor que um corpo precisa para variar sua temperatura em uma unidade. Matematicamente é equivalente:
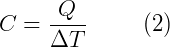
onde ΔT é a variação de temperatura, Q é a quantidade de calor e C a capacidade térmica, esta última em cal/ºC (calorias por graus Celsius) ou J/K (Joule por Kelvin).
Definidos estes conceitos, podemos determinar a quantidade de calor. Sabe-se, experimentalmente, que a quantidade de calor é proporcional a
- massa m
- variação de temperatura ΔT
Assim,
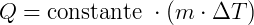
a constante de proporcionalidade na equação é o calor sensível c da substância (também chamado de calor específico). Portanto a quantidade de calor Q será:
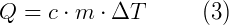
A equação 3 é conhecida como a equação fundamental da calorimetria, devido a sua importância no cálculo da quantidade de calor. Ela foi determinada experimentalmente.
Imagine agora vários corpos em um ambiente isolado, ou seja, que não troca massa nem energia com o ambiente externo (uma caixa de isopor, por exemplo). Se estes corpos estiverem com suas temperatura diferentes entre si, haverá trocas de calor até que haja um equilíbrio térmico dentro deste sistema.
Como o sistema está isolado, a energia térmica total no seu interior deverá ser constante, independente das trocas alí dentro efetuadas. Pelo princípio da conservação da energia, temos o seguinte enúnciado do balanço energético:
"A soma das quantidades de calor cedidas por uns corpos é igual à soma das quantidades de calor recebidas pelos demais corpos".
Ou seja,
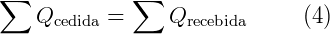
se utilizarmos como convenção que o calor recebido será positivo (Q > 0) e o calor cedido será negativo (Q < 0), teremos
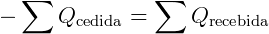

O balanço energético visto acima é útil no descobrimento de variáveis desconhecidas no sistema.
É importante destacar, ainda, que em um mesmo corpo podem ocorrer as duas formas de recebimento ou doação de calor: o sensível e o latente. Suponhamos, por exemplo, um cubo de gelo que recebe calor latente o suficiente para se tornar líquido e, ao continuar recebendo calor (sensível agora), começa a esquentar a água, a qual ele se tornou. Assim, a quantidade de calor total recebida por este bloco de gelo será:
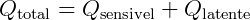
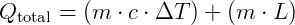
Sendo o calor total recebido a soma dos calores latente do gelo e sensível da água.
Texto originalmente publicado em https://www.infoescola.com/fisica/calorimetria/
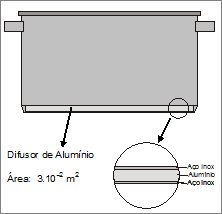 O tipo de panela mais recomendado, por questões de saúde, é a panela de aço inox. Entretanto, o aço inox tem uma baixa condutividade térmica. Para solucionar este problema, os fabricantes fazem uso de um difusor de calor, geralmente de alumínio, cujo objetivo é melhorar a condutividade e homogeneizar a transferência de calor no fundo da panela.
O tipo de panela mais recomendado, por questões de saúde, é a panela de aço inox. Entretanto, o aço inox tem uma baixa condutividade térmica. Para solucionar este problema, os fabricantes fazem uso de um difusor de calor, geralmente de alumínio, cujo objetivo é melhorar a condutividade e homogeneizar a transferência de calor no fundo da panela.