Os conceitos de quente e frio são recorrentes em nosso cotidiano. Apesar de o conceito de frio ser fisicamente inexistente, ao mesmo se atribui uma temperatura menor em relação a outro sistema em análise. Por exemplo, em uma sala com o ar condicionado ligado onde a temperatura é 25°C e a temperatura externa for 30°C , habitualmente se coloca aquele ambiente como mais frio com relação a este. Fisicamente, falamos em temperaturas (medidas de agitação das moléculas) diferentes. Dentro das Ciências Física, há um ramo de estudos que estuda a Energia Térmica e suas relações com o meio: A Termologia (termo = calor, logia = estudo).
 De acordo com o Dicionário Houaiss de Física, Termologia é o ramo da Física que estuda o calor. Atualmente, os materiais didáticos têm colocado o termo como equivalente de Física Térmica ou Termofísica.
De acordo com o Dicionário Houaiss de Física, Termologia é o ramo da Física que estuda o calor. Atualmente, os materiais didáticos têm colocado o termo como equivalente de Física Térmica ou Termofísica.
Dois conceitos fundamentais para este ramo de estudos (e que, corriqueiramente, são confundidos pelas pessoas) são calor e temperatura.
É um fato conhecido que os corpos são constituídos de elementos menores: átomos e moléculas. Ainda, que estas partículas encontram-se em contínuo movimento. O estudo acerca deste movimento foi feito por Albert Einstein e é conhecido como Movimento Browniano.
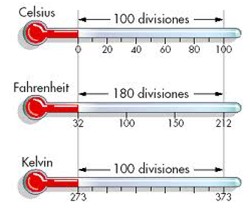 Com base nisso, pode-se inferir que temperatura é uma grandeza que mede o estado de agitação das partículas de um corpo, caracterizando o seu estado térmico, ou seja, quantificando a sua Energia Cinética Média. Para medir a temperatura dos corpos utiliza-se o termômetro. As escalas utilizadas são o Celsius (em homenagem ao Físico Anders Celsius), Fahrenheit (homenagem a Gabriel Daniel Fahrenheit) e Kelvin (homenagem e Willian Thomson – o Lord Kelvin).
Com base nisso, pode-se inferir que temperatura é uma grandeza que mede o estado de agitação das partículas de um corpo, caracterizando o seu estado térmico, ou seja, quantificando a sua Energia Cinética Média. Para medir a temperatura dos corpos utiliza-se o termômetro. As escalas utilizadas são o Celsius (em homenagem ao Físico Anders Celsius), Fahrenheit (homenagem a Gabriel Daniel Fahrenheit) e Kelvin (homenagem e Willian Thomson – o Lord Kelvin).
A escala de Celsius, por sua simplicidade, se tornou praticamente universal. Durante muito tempo, foi chamada de escala centígrada, mas em 1948, por convenção internacional, decidiu-se mudar seu nome para escala Celsius. Com isso, a escala de Kelvin se constitui, atualmente, como padrão internacional.
Por Calor podemos entender que é forma de energia em trânsito de um corpo de maior temperatura para outro de menor temperatura. Estabeleceu-se como unidade de quantidade de calor a caloria (cal) – a quantidade de calor necessária para aumentar a temperatura de um grama de água de 14,5ºC a 15,5ºC, sob pressão normal (1 atm).Contudo, para o Sistema Internacional de unidades a unidades de quantidade de calor é o Joule (J), em honra ao Físico James Prescott Joule (1818 - 1889). A relação entre a caloria e o Joule (chamada de equivalente mecânico) é: 1 cal = 4,186 J.
Um exemplo de aplicação dos conhecimentos adquiridos na Termologia pode ser vista no seguinte vídeo:
Fontes:
Dicionario Houaiss De Fisica. Itzhak Roditi,Instituto Antonio Houaiss.
Física General. Sears e Zemansky. Aguilar. Madrid.
Fundamentos de Física. Resnick, Halliday e Walker. Vol. 2. LTC. 4ª Edição. LTC. RJ. 1996.
Texto originalmente publicado em https://www.infoescola.com/fisica/termologia/