“Propriedades físicas” é uma expressão de significado muito amplo: engloba todas as propriedades das substâncias relacionadas a fenômenos físicos. Não teria nenhum sentido tentar estudar todas as propriedades físicas de uma vez; apenas para enumerá-las todas já seriam consumidas um espaço enorme. Em geral estabelecemos objetivos de natureza prática para delimitar nossos estudos: as propriedades físicas que nos interessam neste momento são aquelas que utilizamos corriqueiramente nos trabalhos comuns de laboratório, como ponto de fusão, ponto de ebulição, solubilidade. Estas propriedades estão fortemente associadas com as forças que mantêm as moléculas unidas umas com as outras, chamadas forças intermoleculares.
Forças intermoleculares
A ligação que prende os átomos dentro de uma molécula é a ligação covalente. As forças de atração entre as moléculas são de natureza elétrica. Forças gravitacionais também existem, mas podemos desprezá-las por serem muito menores do que as forças elétricas. Vamos, agora, analisar as forças que existem entre as moléculas.
Essas forças podem ser divididas em dois tipos: forças de Van der Waals e Ligação de Hidrogênio.
Forças de Van der Waals
As forças de atração ou repulsão entre entidades moleculares (ou entre grupos dentro da mesma entidade molecular) diferentes daquelas que são devidas à formação de ligação ou a interação eletrostática de íons ou grupos iônicos uns com os outros ou com moléculas neutras.
Vamos estudar dois tipos principais:
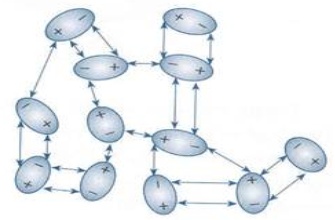
Força entre dipolos permanentes: Se a molécula da substância contém um dipolo permanente (devido à polaridade de uma ou mais de suas ligações covalente), então podemos facilmente ver como essas moléculas se atraem umas às outras: o lado positivo do dipolo de uma molécula atrai o lado negativo do dipolo da outra molécula. Esta força existe, portanto, entre moléculas polares (μtotal ≠ 0).
Exemplo:
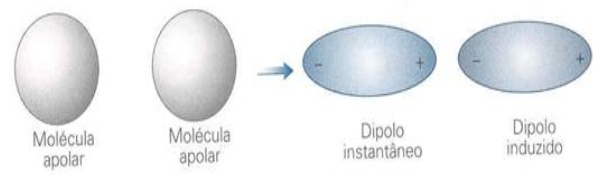
Forças de London ou forças de dispersão: E quando as moléculas não contêm dipolos (são apolares), como é que elas podem se atrair? Pense numa molécula como uma entidade não estática, mas contendo elétrons em constante movimento; é razoável pensar que num determinado momento a distribuição nessa molécula pode não ser perfeitamente simétrica, e apareçam então pequenos dipolos instantâneos neste momento. Esses dipolos desaparecerão em muito pouco tempo, podendo levar a uma molécula neutra ou a outros dipolos, inclusive contrários; mas no curto espaço de tempo em que eles existem, eles podem induzir a formação de dipolos contrários na molécula vizinha, levando as duas a se atraírem mutuamente. Exemplo:
Ligações de Hidrogênio: O átomo de hidrogênio tem propriedades especiais por ser um átomo muito pequeno, sem elétrons no interior: por dentro da camada de valência há apenas o núcleo do átomo, o próton. Uma das propriedades que só o átomo de hidrogênio apresenta é a capacidade de exercer uma força de atração intermolecular chamada ligação de hidrogênio. A ligação de hidrogênio só pode ocorrer quando o hidrogênio estiver ligado a um átomo pequeno e muito eletronegativo, como F, O, N, Cl, etc. Quando o hidrogênio está ligado a um átomo muito eletronegativo, a densidade eletrônica em torno do próton fica bem baixa; esta parte da molécula é então fortemente atraída pelos pares de elétrons do átomo eletronegativo de outra molécula, estabelecendo a ligação de hidrogênio.
Exemplo:
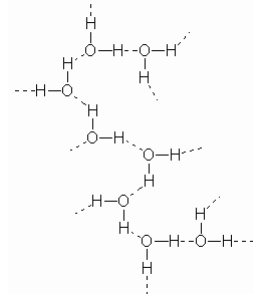
As ligações de hidrogênio representam importante papel tanto nas propriedades especiais da água como em moléculas de extrema importância para os seres vivos: elas determinam a forma das proteínas, e constituem a força que une as hélices do DNA.
Texto originalmente publicado em https://www.infoescola.com/quimica/forcas-intermoleculares-van-der-waals-e-ponte-de-hidrogenio/