Os haletos são compostos químicos que possuem qualquer um dos representantes da família 7A (flúor, cloro, bromo, iodo e astato) com estado de oxidação -1. Sendo que, a reação de síntese dessas espécies pode ser tanto com os halogênios puros (em estado molecular: F2, Cl2) ou com ácidos HX (sendo X o respectivo íon: F-, Cl-). Que, por serem muito eletronegativos, têm facilidade de se ligar até aos gases nobres (como fluoretos de xenônio – XeF2, XeF4, XeF6 – mesmo que por um curto espaço de tempo).
Haletos Inorgânicos
Neste grupo se encaixam os haletos de hidrogênio (que em meio aquoso se tornam ácidos de Arrhenius, liberando íons H+ e X- - HF, HCl, HI, HBr. Apenas o astato não forma compostos conhecidos, até por que a quantidade existente na crosta terrestre não passa de 30 gramas; e os sais inorgânicos (formados pela atração eletrostática entre os ânions mencionados e cátions metálicos. Podendo ser produzidos por reação de neutralização, por exemplo).
- HF(aq) + NaOH(aq) → NaF(aq) + H2O(l)
- 2HI(aq) + Ca(OH)2(aq) → CaI2(aq) + 2H2O(l)
- 2HCl(aq) + Mg(OH)2(aq) → MgCl2(aq) + 2H2O(l)
Os haletos inorgânicos também podem ser exemplificados por complexos metálicos, a exemplo do iodeto de mercúrio II (HgI2) que sob excesso de iodeto (I-) forma o íon tetraiodomercurato (HgI42-), utilizado na determinação qualitativa da amônia (titrimetria de complexação).
Ou ainda, na titrimetria de precipitação, os íons cloreto, brometo e iodeto são determinados através da reação com a prata (formando compostos insolúveis – apenas o fluoreto forma composto solúvel):
- NaCl(aq) + AgNO3(aq) → AgCl(s) + NaNO3(aq)
- KBr(aq) + AgNO3(aq) → AgBr(s) + KNO3(aq)
- KI(aq) + AgNO3(aq) → AgI(s) + KNO3(aq)
Haletos Orgânicos
Recebem essa classificação as moléculas orgânicas que possuem átomos de halogênio na sua estrutura (também via fornecimento molecular ou sob forma de HX – geralmente com a substituição de algum átomo de hidrogênio da cadeia, caso seja constituída apenas por ligações simples – cadeia saturada).
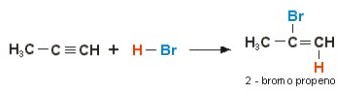
A reação de halogenação pode ocorrer com a formação, ou não, de haletos de hidrogênio (ácidos de Arrhenius, caso se encontrem em meio aquoso). Para a previsão de tal característica, deve-se observar a insaturação das ligações da molécula a ser halogenada e a forma na qual o halogênio está disponível: caso esteja sob forma molecular e a cadeia possua pelo menos uma ligação insaturada, não há formação de HX como produto da reação (halogenação por adição); entretanto, se a cadeia for saturada ou for anel benzênico, há formação de HX (halogenação por substituição – de um átomo de halogênio por um de hidrogênio).
Halogenação por adição:
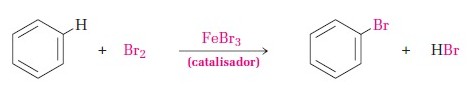
Halogenação por substituição:
Texto originalmente publicado em https://www.infoescola.com/quimica/haletos/