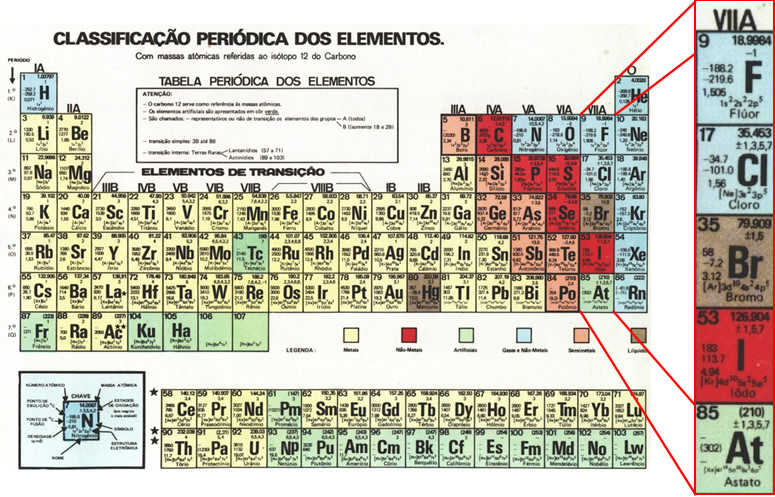
O grupo dos halogênios é o de número 17 (ou 7A) da tabela periódica e tem seu nome derivado do grego e que significa formadores de sais. Todos os elementos desta família são não metais (ametais) e representativos. São eles: flúor, cloro, bromo, iodo, astato e ununséptio. A distribuição eletrônica deles acaba sempre no subnível p e com 5 elétrons. Este grupo possui como uma de suas principais características a alta eletronegatividade que é a tendência que certo elemento possui de atrair elétrons para si, sendo o de maior eletronegatividade o flúor (F). Na natureza aparecem sempre na forma diatômica, por exemplo: Cl2 e F2.
Sempre que recebem um elétron em uma ligação, ficam com carga negativa advinda deste elétron e então os chamamos de haletos. Quando os halogênios formam sais chamamos de sais de haleto, exemplos disso são o cloreto de sódio (NaCl) e o fluoreto de sódio (NaF2).
Quando ligados entre si formam ligações covalentes e quando ligados com metais formam ligações iônicas. O flúor é encontrado na forma gasosa assim como o cloro. O bromo é encontrado no estado líquido, o astato e o iodo são sólidos. O ununséptio é um elemento transurânico e sintético obtido a partir de um acelerador de partículas. Provavelmente é sólido e possui cor escura.
Aplicações no cotidiano
O flúor pode ser encontrado no creme dental que utilizamos, e é extremamente corrosivo ao vidro devendo sempre ser armazenado em outro tipo de recipiente. O cloro é utilizado no tratamento da água das piscinas e também está presente no sal de cozinha na forma de cloreto. Lembrando sempre que ele deve ser utilizado em quantidades pequenas em caixas de água e piscinas devido à tendência a agredir as vias aéreas quando utilizado sem moderação, podendo causar complicações. Além disso também é parte da composição de produtos que possuem poder clareador como por exemplo os produtos que tiram manchas de tecidos.
O cloro e o flúor são também contribuintes para o aumento do efeito estufa na forma de clorofluorcarbonetos (CFC’s) - antigamente utilizados em aerossóis.
O bromo é encontrado em produtos destinados à exterminação de insetos na forma de brometo. O iodo é parte da composição do sal de cozinha sendo utilizado para evitar o bócio, uma doença que ataca a glândula da tireoide, porém também não deve ser consumido em excesso. Ele é o único deste grupo que não é tóxico e juntamente com o cloro possui ação antimicrobiana e antibacteriana. O astato ainda não possui aplicação, sendo apenas objeto de estudo teórico por enquanto bem como o ununséptio.
Texto originalmente publicado em https://www.infoescola.com/quimica/halogenios/