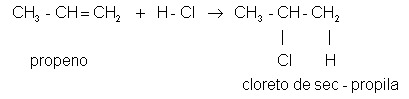As reações de halogenação referem-se àquelas onde um átomo de qualquer elemento da família 7A (halogênios – F, Cl, Br e I) substitui um átomo de hidrogênio, ou ainda, reduz a insaturação de uma ligação entre carbonos (pela eliminação de uma ligação pi).
A halogenação pode se apresentar como uma substituição (quando realmente um átomo de hidrogênio dá lugar a um de halogênio) ou adição (quando reduz o número de ligações pi entre carbonos e preserva o número de átomos de hidrogênio).
Halogenação por Adição
Moléculas orgânicas que possuem, pelo menos, uma ligação insaturada (dupla ou tripla) participam de reações de adição quando em contato com halogênios (sob sua forma molecular ou como haletos de hidrogênio – HX).
De acordo com a regra de Markovnikov, ao adicionar um haleto de hidrogênio do tipo HX, o hidrogênio liga-se ao carbono mais hidrogenado da ligação insaturada. Ao ponto que o halogênio liga-se ao outro carbono (menos hidrogenado).
Como exemplo, observe a reação de adição entre o propileno (propeno – de acordo com a nomenclatura da IUPAC) e cloreto de hidrogênio:
Assim como é prevista pela regra de Markovnikov, o hidrogênio da molécula de HCl liga-se ao carbono 1 da molécula de propeno (mais hidrogenado da ligação dupla), enquanto que o cloro liga-se ao carbono 2 (secundário).
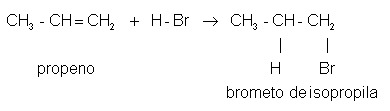
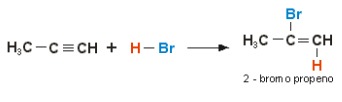
Entretanto, nem sempre a regra de Markovnikov é seguida. Um exemplo é a formação do brometo de isopropila, onde o hidrogênio da molécula de HBr liga-se ao carbono secundário (menos hidrogenado da insaturação):
Quando a espécie a ser halogenada é um alcino, poderá ser formado um produto duplamente halogenado (dihaleto) caso o reagente HX esteja em excesso.
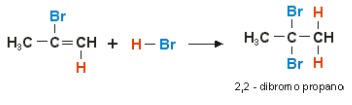
O esquema abaixo representa a halidrificação (adição de HX) de uma molécula de metil-acetileno com brometo de hidrogênio em excesso:
 Como ainda há brometo de hidrogênio no meio, ocorre outra reação de halogenação por adição de HBr:
Como ainda há brometo de hidrogênio no meio, ocorre outra reação de halogenação por adição de HBr:
Halogenação por Substituição
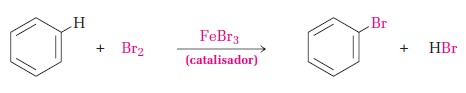
Quando um alcano ou aromático reage com uma molécula de halogênio, ocorre a denominada reação de substituição. Pois, apenas um dos átomos da molécula halógena se liga à molécula orgânica. Assim, um hidrogênio migra e um haleto de hidrogênio é formado como produto.
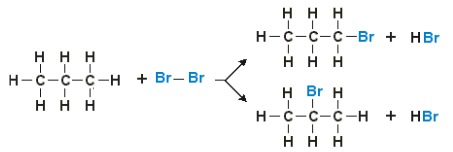
Observe o exemplo da bromação de uma molécula de propano:
Como pode ser visto, dois produtos diferentes (isômeros) podem ser obtidos. Entretanto, pode-se inferir que a segunda forma é a mais abundante: pois, é obtido experimentalmente que há aumento da tendência do hidrogênio ser substituído quando há aumento do número de ligações saturadas de um átomo de carbono. Assim, um hidrogênio ligado a um carbono terciário tem maior possibilidade de ser substituído por um halogênio em relação a um hidrogênio de carbono secundário ou primário da mesma molécula.
Nos aromáticos, a halogenação raramente ocorre na falta de catalisadores. Pois estes auxiliam na “migração” do halogênio através de um ataque eletrófilo ao anel (de acordo com a teoria ácido-base de Lewis):
Bibliografia:
PERUZZO, Francisco Miragaia. CANTO, Eduardo Leite. Química na Abordagem do Cotidiano: Química Orgânica, São Paulo. Moderna, 2006. 4ª edição.
https://web.archive.org/web/20100702053821/http://www.moderna.com.br:80/didaticos/em/quimica/cotidiano/aluno/qui_organica/mec03.pdf (acesso em 14/08/2010)
https://web.archive.org/web/20100922081132/http://www.ebah.com.br:80/halogenacao-doc-a51705.html (acesso em 14/08/2010)
https://web.archive.org/web/20180804041758/http://soq.com.br:80/conteudos/em/reacoesorganicas/p1.php (acesso em 14/08/2010)
Texto originalmente publicado em https://www.infoescola.com/reacoes-quimicas/halogenacao/