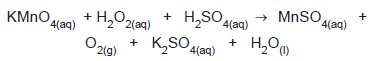As principais classes de reações estudadas no Ensino Médio são as de precipitação, ácido/base e oxirredução. Esta última abrange uma série de reações muito versáteis e importantes, como a combustão, a corrosão, a fotossíntese, a extração de minérios, entre outras. Reações de oxirredução são também chamadas de oxidorredução ou redox, pois trata-se da combinação de semirreações de oxidação (em que ocorre perda de elétrons) e de redução (em que há ganho de elétrons), assim, pode-se dizer que reações desse tipo tratam da migração de elétrons de uma espécie a outra.
Sempre que houver uma oxidação, haverá também uma redução, pois, como elétrons são partículas reais, que não podem ser simplesmente "perdidas" (já que na natureza "nada se perde, nem se cria", segundo Lavoisier), quando uma espécie perder elétrons, outra espécie necessariamente irá ganhá-los, assim, sempre que uma espécie oxidar, outra irá reduzir.
Por exemplo, em uma das etapas da formação da ferrugem, o ferro sólido é oxidado pelo ar úmido (O2 + H2O), e pode ser descrita da seguinte maneira:
Semirreação de oxidação: 2Fe(s) → 2Fe2+(s) + 4e-
Semirreação de redução: O2(g) + 2H2O(l) + 4e- → 4OH-(aq)
________________________________________________
Reação global: 2Fe(s) + O2(g) + 2H2O(l) → 2Fe(OH)2(s)
Neste caso, a espécie que está oxidando (perdendo elétrons) é o ferro, enquanto que quem está reduzindo (ganhando elétrons) é o oxigênio do O2. A espécie que oxida é chamada de agente redutor, pois é quem provoca a redução da outra espécie. Da mesma forma, quem sofre redução é chamado de agente oxidante. Assim, neste exemplo dado, o Fe(s) é agente redutor e O2(g) agente oxidante.
É daí que vem o termo "antioxidante", produtos antioxidantes são aqueles que possuem substâncias capazes de atrasar ou inibir a oxidação de algum material e, portanto, podem ser agentes redutores. As reações de oxidação, embora sejam normais (e essenciais) nos organismos vivos, podem produzir radicais livres, potencialmente perigosos a estes organismos. Acredita-se que muitas doenças, como Alzheimer, Parkinson, diabetes, alguns tipos de câncer, dentre outras e até o envelhecimento da pele estejam atreladas a um "estresse oxidativo" (excesso de oxidação, por assim dizer) e por isso, remédios e alimentos antioxidantes, como uva, maçã, brócolis, linhaça, etc. são consumidos como formas de prevenção.
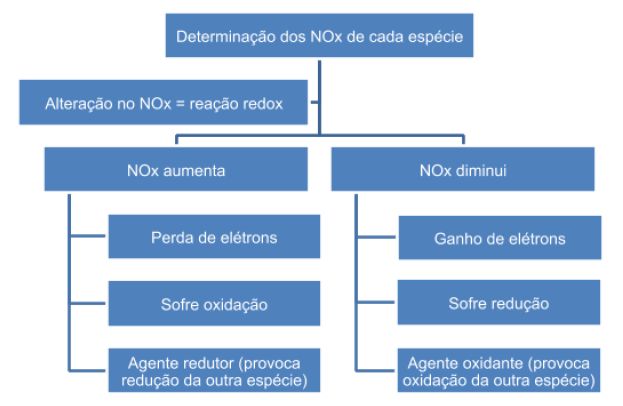
Para verificar se uma reação é do tipo redox, basta identificar se há variação no número de oxidação (NOx) das espécies envolvidas: se houver diminuição do NOx, significa que a espécie sofreu redução, se houver aumento, oxidação e, portanto, trata-se de uma oxirredução. A espécie que sofreu redução é o agente oxidante, e a que sofreu oxidação, agente redutor. A seguir, um fluxograma para resumir essas informações:
Texto originalmente publicado em https://www.infoescola.com/quimica/oxirreducao/