Por Ricardo Normando Ferreira de Paula
Em 1922 Neils Bohr recebeu o prêmio Nobel por suas contribuições na Teoria Atômica. A partir daí (esta é uma data de referência) vários cientistas empreendem uma corrida cujo intuito é penetrar cada vez mais no interior do átomo e desvendar os mistérios que envolvem este segmento da matéria.
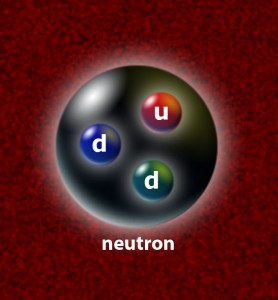 Uma das grandes questões que havia era se, além do próton, existiam outras partículas no núcleo e como elas deveriam se comportar. A problemática era subjacente ao seguinte fato: o núcleo de Hidrogênio tem metade da carga de um núcleo de Hélio, no entanto o Hélio tem o quádruplo da massa do Hidrogênio. A mesma relação se repete para o Carbono e o Oxigênio, além de outros átomos estudados na época. Qual o motivo desta relação?
Uma das grandes questões que havia era se, além do próton, existiam outras partículas no núcleo e como elas deveriam se comportar. A problemática era subjacente ao seguinte fato: o núcleo de Hidrogênio tem metade da carga de um núcleo de Hélio, no entanto o Hélio tem o quádruplo da massa do Hidrogênio. A mesma relação se repete para o Carbono e o Oxigênio, além de outros átomos estudados na época. Qual o motivo desta relação?
Desde 1920, Ernest Rutherford já “previa” a existência de partículas grandes e sem carga (daí o nome Nêutron) em seus estudos. A partir daí empreende estudos na tentativa de comprová-los. Apesar de seus esforços, James Chadwick, seu aluno, é quem consegue confirmar a existência do nêutron a partir dos estudos de Irène Curie e Frédéric Juliot (filha e genro do casal Curie), os quais descobriram um tipo de radiação altamente energética, contudo sem carga. Este fato foi decisivo na descoberta de Chadwick. Irène e Juliot estavam pesquisando acerca do bombardeio de Berílio com partículas alfa. Acreditavam, erroneamente, havia como resultado partículas alfa, no entanto Chadwick esclarece a presença do nêutron na situação, o que lhe rendeu o prêmio Nobel de Física de 1935.
A descoberta do aluno de Rutherford dá um passo extremamente importante no estudo do núcleo atômico e, consequentemente, abre discussões acerca do que pode ainda haver nesta misteriosa região.
A massa inercial de um Nêutron é 1,008664904 unidades de massa atômica, cerca de 0,1% mais pesado que o próton.
Como a carga de um Nêutron é nula, sua interação com campos eletromagnéticos é desprezível. Sendo assim, a sua interação com a matéria se dá com a interação direta entre os núcleos o que o faz uma “peça chave” quando se pretende investigar acerca de núcleos atômicos sem a interferência das camadas.
De acordo com a literatura, estas partículas são classificadas em três faixas (de acordo com a sua energia cinética): nêutrons térmicos, nêutrons epitérmicos e nêutrons rápidos.
Os dois usos tecnológicos mais conhecidos do nêutron são a bomba atômica e os reatores nucleares, ambos fundamentados no evento da fissão nuclear.
Leia também:
Referências:
Livro: As sete maiores descobertas científicas da história e seus autores de David Eliot Brody,Laura Teixeira Motta;
Fundamentos da física de nêutrons de Cibel Bugo Zamboni (org.)
Texto originalmente publicado em https://www.infoescola.com/fisica-nuclear/neutron/