Um sal é todo composto obtido a partir da reação química entre um ácido orgânico e uma base, a qual resultará em um sal orgânico (1), ou entre um ácido inorgânico e uma base, a qual resultará em um sal inorgânico (2). As reações de obtenção de sais, tanto de natureza orgânica ou inorgânica, recebem o nome de reações de neutralização.
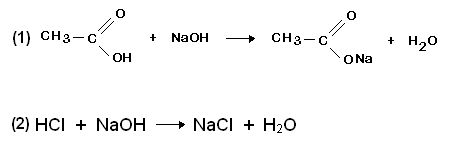
- (1) Ácido etanóico (ácido acético) reage com hidróxido de sódio e produz acetato de sódio (exemplo de sal orgânico) e água.
- (2) Ácido clorídrico reage com hidróxido de sódio e produz cloreto de sódio (exemplo de sal inorgânico) e água.
Um sal também pode ser definido como toda substância que, em meio aquoso, se dissocia, liberando um cátion diferente de H+ e um ânion diferente de OH-, conforme pode ser visto abaixo na dissociação do sal cloreto de magnésio (MgCl2), que dá origem ao cátion Mg2+ e ao ânion cloreto (Cl-).
De acordo com seu comportamento experimental, um sal inorgânico pode ser classificado em:
- Sal neutro: composto resultante da reação de neutralização onde todos os hidrogênios ionizáveis do ácido foram neutralizados sem excesso pelas hidroxilas da base. Não apresentam H+ nem OH- em sua fórmula molecular. Por exemplo, temos o fluoreto de cálcio (CaF2) e o brometo de potássio (KBr).
- Sal ácido: composto resultante da reação de neutralização onde nem todos os hidrogênios ionizáveis do ácido foram neutralizados pelas hidroxilas da base. Apresentam H+ em sua fórmula molecular. São reconhecidos também por hidrogeno-sal; é formado por mais de um cátion. Por exemplo, temos o mono-hidrogeno sulfato de sódio (NaHSO4) e o bicarbonato de sódio (NaHCO3).
- Sal básico: composto resultante da reação de neutralização onde nem todas as hidroxilas dissociáveis da base foram neutralizadas pelos hidrogênios do ácido. Apresentam OH- em sua fórmula molecular. São reconhecidos também por hidróxi-sal; é formado por mais de um ânion. Por exemplo, temos o cloreto monobásico de alumínio (Al(OH)Cl2) e o fluoreto monobásico de cálcio (Ca(OH)F).
- Sal misto: composto que apresenta dois ânions diferentes, onde nenhum deles é OH-, ou dois cátions diferentes, onde nenhum deles é H+. Por exemplo, temos o sulfato de sódio e potássio (NaKSO4).
- Sal hidratado: apresentam moléculas de água dando configuração a seu retículo cristalino. O mais comum é o sulfato de cobre penta hidratado (CuSO4.5H2O), o qual apresenta coloração azul no estado sólido ou em meio aquoso devido às suas cinco moléculas de água de hidratação.
Referências:
ATKINS, Peter; JONES, Loreta; Princípios de Química: questionando a vida moderna e o meio ambiente, Porto Alegre: Bookman, 2001.
FELTRE, Ricardo; Fundamentos da Química, vol. Único, Ed. Moderna, São Paulo/SP – 1990.
PERUZZO, Francisco Miragaia (Tito); CANTO, Eduardo Leite; Química na Abordagem do Cotidiano, Ed. Moderna, vol.1, São Paulo/SP- 1998.
Texto originalmente publicado em https://www.infoescola.com/quimica/classificacao-de-sais-inorganicos/