O peróxido de hidrogênio (H2O2) pertence à classe dos peróxidos e é caracterizado por ser um composto binário formado pela ligação entre o hidrogênio e oxigênio, na forma de O22-, sendo que neste composto o oxigênio esta no estado de oxidação -1. É um composto inorgânico molecular encontrado no estado líquido na temperatura ambiente, e cuja interação intermolecular é feita através de ligações hidrogênio. É um líquido incolor, viscoso, solúvel em água, e quando não está dissolvido se decompõe rapidamente, sendo bastante instável, pelo fato de suas ligações serem fracas, com energia de ligação de 144 kJ/mol.
Sua reação de decomposição libera gás oxigênio e água.
2 H2O2 → 2 H2O + O2
É um composto bastante oxidante quando está na presença de compostos redutores e quando oxidado forma moléculas de água.
H2O2 + 2H+ → 2H2O
Entretanto pode agir também como redutor ao reagir com oxidantes fortes e os produtos da reação são água e oxigênio.
H2O2 + 2OH- → O2+ H2O
Não é uma substância inflamável, porem pode sofrer combustão espontânea na presença de matéria orgânica ou alguns metais como o cobre ou o bronze.
Foi descoberto por Louis Jacques Thénard, após uma reação de peróxido de bário com ácido nítrico:
BaO2 + 2HNO3 → H2O2 + Ba(NO3)2
Atualmente é produzido industrialmente a partir do equilíbrio entre os compostos antraquinol e antraquinona, em uma reação feita na presença de oxigênio e hidrogênio.
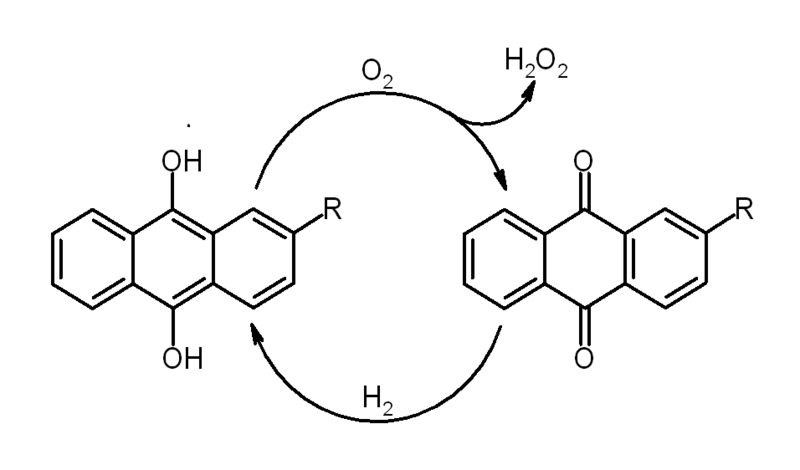
Figura 1: Equilíbrio antraquinol e antraquinona.
Após o término da reação, o peróxido produzido é extraído com água e feita uma destilação a pressão reduzida, para concentrar a amostra.
O peróxido de hidrogênio tem diversas aplicações que variam de acordo com a concentração da solução. Em nosso cotidiano, por exemplo, encontramos soluções com concentrações de H2O2 menores que 8% (m/v), entre eles, creme dental (0,5% (m/v)), detergentes para lente de contato (2% (m/v)), produtos para branqueamento (5% (m/v)) e loções para clareamento de cabelo (7,5% (m/v)). No setor industrial temos aplicação de soluções com concentrações entre 8 e 27,5% (m/v) que são utilizadas para clarear tecidos, papel, fabricação de espuma de borracha sintética e poliuretano. Além disso, encontram aplicação como oxidante de matéria orgânica e metais, no processo de tratamento de efluentes. Soluções com concentrações superiores a 27,5 % (m/v) tem aplicações em processos mais específicos e requerem muito cuidado no manuseio, pois algumas são altamente corrosivas ou sofrem decomposições explosivas. Soluções com concentrações superiores a 91 % (m/v) são empregadas em propulsores de foguetes.
Dentro do nosso organismo, em um processo de oxidação natural, o H2O2 pode ser formado em quantidades bem pequenas. Para que não causem nenhum tipo de prejuízo, nosso metabolismo dispõe da enzima catalase, que promove a decomposição em H2O e O2 elementar. Quando utilizamos solução de água oxigenada para limpar ferimentos, ele se decompõe em contato com nossa pele, com isso mata bactérias e vírus anaeróbicos (que não sobrevivem à presença de oxigênio), tendo por isso uma função desinfetante. Vale ressaltar aqui que água oxigenada não é sinônima de peróxido de hidrogênio, uma vez que esse produto comercial tem concentrações por volta de 3% (m/v) e 6% (m/v), que correspondem a informação mais comumente descrita nos rótulos de 10 e 20 volumes. Já o termo peróxido se refere ao composto puro.
Referencias
Atkins, P. W.; Jones, Loretta . Princípios de química: questionando a vida moderna e o meio ambiente. Volume único. 3. ed. Porto Alegre: Bookman, 2006.
Kotz, J. C. Química Geral e Reações Químicas. Volume 1, 9ª edição, Cengage Learning, 2015.
Mattos, L. I. ; Shiraishi, K. A.; Delphini, B.; Fernandes, J. F. Peróxido de Hidrogênio: importância e determinação. Química Nova, vol 26, n.3. Maio, 2003.
Tito e Canto. Química na Abordagem do Cotidiano. Volume único, parte A – Química Geral e Inorgânica. Editora Saraiva 2005.
Texto originalmente publicado em https://www.infoescola.com/quimica/peroxido-de-hidrogenio/