Os polímeros são obtidos através de uma ou mais reações químicas chamadas Reações de Polimerização. A palavra “Polimerização” significa Poli: várias e Meros: partes, ou seja, é união de vários “meros” que ao final da reação, formam uma cadeia longa chamada polímero, pode ser ainda definida como um conjunto de reações através das quais monômeros reagem entre si, formando macromoléculas poliméricas.
Essas reações ocorrem através de moléculas simples que reagem entre si, formando o que chamamos de macromoléculas. As macromoléculas possuem como principal característica elevada massa molar e após a reação de polimerização, a massa molar deve ser superior a 10.000 g/mol para que o produto formado seja considerado um polímero.
As reações de polimerização utilizam parâmetros primários e secundários para que possam ocorrer, são eles:
- Parâmetros primários: pressão, temperatura de reação, tempo e presença de iniciador de reação;
- Parâmetros secundários: São os itens que são específicos para o polímero a ser produzido, tais como, inibidores, catalisadores, retardadores de reação, controladores de massa molar, reagentes específicos, etc.
A polimerização pode ocorrer em etapas, em cadeia, por abertura de anel ou por copolimerização. A seguir detalharemos cada tipo de polimerização.
Conteúdo deste artigo
Polimerização em etapas
Ocorre pela condensação sequencial de grupos funcionais presentes nos monômeros, formando através das ligações sucessivas o aumento de tamanho das moléculas até que as mesmas formem uma cadeia polimérica (alta massa molar), esse aumento ocorre no decorrer do tempo da reação. Os grupos funcionais dos monômeros são reativos entre si, não necessitando de iniciadores para que ocorra o start da reação. Há formação de subprodutos resultantes da reação, como por exemplo, H2O, HCl, NH3, etc. A polimerização em etapas sofre influência direta de alguns fatores importantes:
- Temperatura e tempo de reação – quanto maior o tempo de reação há a formação de polímeros com maiores massas molares;
- Catalisadores – facilitam a reação, formando polímeros com maiores massas molares;
- Relação equimolar dos grupos funcionais dos monômeros – adicionar o mesmo número de moléculas de cada grupo funcional dos monômeros facilita o encontro entre uma ponta da macromolécula de um grupo funcional com outra ponta de outro grupo funcional, facilitando a reação, aumentando a velocidade da mesma e formando polímeros com maior massa molar ;
- Adição de terminadores – pode ocorre quando houver adição não equimolar dos grupos funcionais, facilitando o encontro entre pontas das macromoléculas com mesmo grupo funcional, que dificulta a polimerização.
Pode ocorrer a terminação da reação através da adição de um reagente monofuncional que torna a ponta da cadeia não reativa, encerrando a polimerização, ou ainda, pode-se reduzir a temperatura de reação, promovendo a redução da velocidade de reação e consequentemente interrompendo a mesma.
Polimerização em cadeia
Ocorre pela instabilização das duplas ligações presentes nos monômeros, ativando uma reação em cadeia (origem do nome da reação), onde cada monômero se liga a outro monômero, onde ocorre a ruptura da dupla ligação, gerando um polo positivo chamado sítio ativo, atraindo assim outros monômeros, e consequentemente continuando com a reação. A reação pode ser representada pela equação genérica abaixo:
n Monômero → [-monômero-]n
Para que ocorra a ruptura da dupla ligação, utiliza-se de reagentes químicos conhecidos como iniciadores termicamente instáveis (I-I•) ou pode-se utilizar também radiações eletromagnéticas, os quais são definidos de acordo com o polímero a ser formado. A reação em cadeia com uso de iniciadores ocorre em três etapas: Iniciação, Propagação e Término.
Na etapa de Iniciação há a adição dos monômeros juntamente com o iniciador, formando espécies químicas reativas (após a ruptura da dupla ligação dos monômeros) que podem ser radicais livres ou íons. Exemplo:
I-I• + CH2=CH2 → R–CH2–CH2•
Na etapa de Propagação, o sítio ativo reage com outros monômeros disponíveis no meio, formando um novo sítio ativo, que por sua vez reage com outro monômero e assim sucessivamente. Nesta etapa ocorre a formação das macromoléculas e crescimento das mesmas. Exemplo:
R–CH2–CH2• + CH2=CH2 → R–CH2–CH2–CH2–CH2•
Na etapa de Terminação, utiliza-se um agente terminador (T – T •) para desativar o sítio reativo da molécula, que pode ser uma outra cadeia em crescimento, radical livre, solvente ou íon, monômero inativo, polímero inativo ou ainda alguma impureza que esteja presente no meio. A macromolécula ativa em crescimento une seu sítio positivo a um terminador que está inativo, finalizado a formação de radical livre e finalizando a reação em cadeia. Exemplo:
R–CH2–CH2–CH2–CH2• + •T–T → (R–CH2–CH2–CH2–CH2–T–T)n
Polimerização por abertura de anel
Ocorre pela instabilização de um monômero em forma de anel, promovendo a abertura do anel, formando sítios ativos que dão início à reação. Com a ruptura deste anel, formam-se duas funções distintas nas extremidades da molécula, que ao reagir consigo mesma proporciona a formação de uma macromolécula. A reação pode ser representada pela equação genérica abaixo:
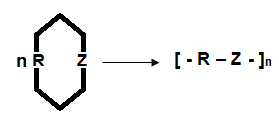
Copolimerização
Ocorre pela união de dois monômeros distintos (m1 e m2), sem interferência externa, ou seja, ocorre naturalmente. De acordo com a reatividade dos monômeros que compõem a reação e de sua respectiva reatividade, pode ocorrer a formação de copolímeros diferentes que possuem seu arranjo estrutural alternado, ao acaso ou em blocos. As possíveis reações podem ser representadas pelas equações genéricas abaixo:
Alternado: n m1• + m2 → (-m1 – m2 – m1 – m2 – m1 -m2 - )n
Ao acaso: n m1• + m2 → (-m1 – m1 – m1 – m2 – m1 -m1 - )n
Em blocos: n m1• + m2 → (-m1 – m1 – m2– m2 – m1 -m1 - )n
Técnicas de Polimerização quanto ao arranjo físico
- Polimerização em massa: Este é o mais simples arranjo físico, onde ao monômero é adicionado o iniciador, iniciando a reação de polimerização, que pode ser caracterizada pelo aumento da temperatura e da viscosidade do meio reacional. Este arranjo proporciona um polímero de alto grau de pureza, porém há dificuldade no controle da temperatura que pode gerar pontos quentes no reator, instabilizando o crescimento das cadeias.
- Polimerização em solução: Neste arranjo físico, visando melhorar a problemática do controle de temperatura, utiliza-se um líquido (solvente) ao meio. Este solvente pode ou não participar da reação (como monômero) de acordo com o produto desejado.
- Polimerização em emulsão: Este arranjo físico é utilizado quando o monômero é um líquido orgânico disperso em água, utilizando um agente emulsificante (sabão) e agitando-se vigorosamente para que as moléculas de sabão formem miscelas hidrofóbicas internamente e hidrofílicas na parte externa, formando como produto final o polímero em forma de pó fino.
Referências:
Canevarolo Jr., Sebastião V. – Ciência dos Polímeros: um texto básico para Tecnólogos e Engenheiros. São Paulo, Editora Artiliber, 2002.
Apostila de Ciência e comportamento dos materiais plásticos I – Núcleo de Tecnologia do Plástico, SENAI SP, 2012.
Texto originalmente publicado em https://www.infoescola.com/quimica/reacao-de-polimerizacao/