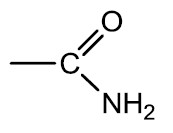
Amidas (função amida) são compostos orgânicos derivados de ácidos carboxílicos pela substituição da hidroxila (‒OH) pelo grupamento amino (‒NH2).
Grupo funcional:
Da mesma forma que as aminas são classificadas em primárias, secundárias e terciárias em função do número de substituintes do hidrogênio do grupo amino, as amidas também recebem essa classificação. As amidas primárias possuem como ligante o ‒NH2, as secundárias têm ligante ‒NHR e as terciárias tem ligante ‒NRR’.
São compostos de caráter básico e polar e por esta razão em geral são solúveis em água pois realizam ligações hidrogênio. Estas ligações de hidrogênio influenciam nas características físicas das amidas, sendo que as primárias tem pontos de fusão e ebulição mais alto o que, em alguns casos, resulta num composto sólido na temperatura ambiente.
Quando uma amida é cíclica ela é conhecida como lactama e sua nomenclatura é dada pelo tamanho do anel: β-lactama para 4 átomos, γ-lactama para 5 átomos e δ-lactama para 6 átomos. As lactamas também podem ser polimerizadas e formar poliamidas.
| β-lactama | γ-lactama |
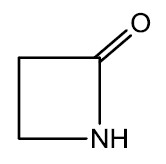 |
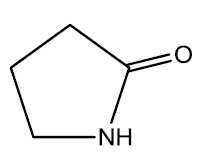 |
| δ-lactama | |
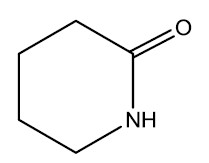 |
|
As amidas são muito empregadas na síntese de polímeros como é o exemplo dos náilons, que são poliamidas encadeadas e também os poliuretanos. Também são empregadas como herbicidas, repelente de insetos e medicamentos.
Conteúdo deste artigo
Nomenclatura das amidas
Nome do hidrocarboneto + AMIDA
| Propanoamida |
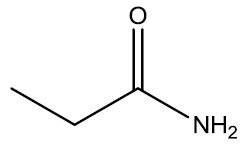 |
| 2-metil-propanoamida |
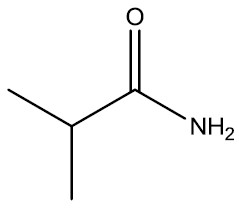 |
Há ainda uma outra maneira de nomear as amidas de forma usual. Esta regra considera o ácido que originou a amida e utiliza-se o prefixo do nome do ácido acrescido da terminação amida.
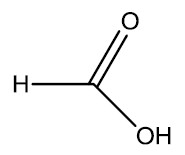 |
⇒ | 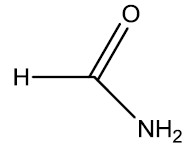 |
| Ácido fórmico | Formamida | |
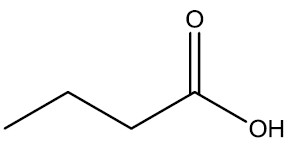 |
⇒ | 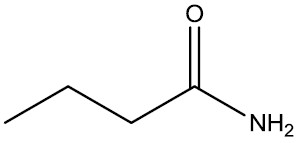 |
| Ácido butírico | Butiramida |
Quando as amidas são secundárias ou terciárias, deve-se colocar o nome dos radicais de hidrocarbonetos ligados ao átomo de nitrogênio antes do nome da amida, colocando a letra N- antes do nome do radical, de forma a deixar claro que este é um substituinte do nitrogênio amídico e não da cadeia hidrocarbônica da amida.
| N-metil-butanamida |
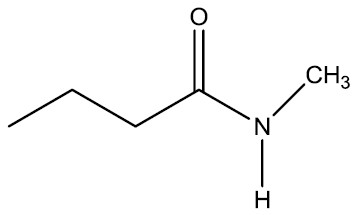 |
| N-etil-N-metil-butanamida |
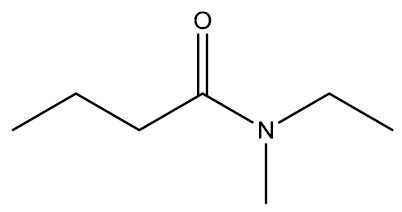 |
Obtenção de amidas
As amidas podem ser sintetizadas em laboratório pela desidratação de sais de amônio (‒NH4), hidratação de nitrilas (‒CN) ou por reações com sais derivados de ácidos.
Algumas amidas importantes
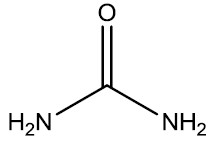
Ureia: é uma diamida do ácido carbônico que é eliminada pela urina por ser produto final do metabolismo dos animais superiores. Se apresenta como um sólido branco, cristalino, solúvel em água e foi o primeiro composto orgânico sintetizado em laboratório. É usada industrialmente como matéria prima na fabricação de fertilizantes e adubos, fabricação de explosivos, resinas e outros compostos orgânicos.
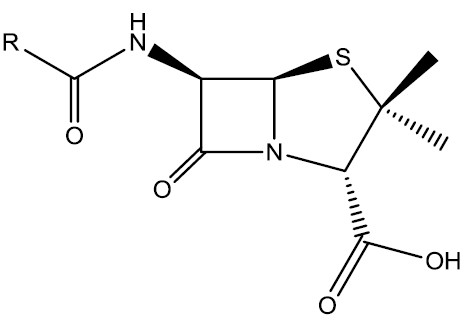
Penicilina: são lactamas utilizadas como medicamentos antibióticos para o tratamento de infecções. São produzidas por fungos do gênero Penicillium e sua atividade antibacteriana se deve ao anel β-lactâmico, de alta reatividade. Foi descoberta pelo médico e bacteriologista escocês Alexander Fleming em 1928, mas só foi utilizada como antibiótico pela primeira vez em 1941.
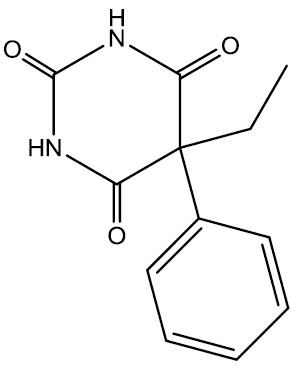
Barbitúricos: são fármacos depressores do sistema nervoso central, constituídos por amidas cíclicas e utilizados como sedativos, hipnóticos, indutores de sono, redutores de ansiedade e no tratamento de distúrbios psíquicos. Seu uso habitual leva a uma tolerância do organismo, exigindo doses cada vez maiores, o que cria dependência. É obtida através de uma reação entre o ácido malônico e a ureia.
Bibliografia:
Atkins, P.W., Jones, L., Princípios de química: questionando a vida moderna e o meio ambiente 5ª ed., Porto Alegre: Ed. Bookman, 2012.
Usberco J., Salvador E., Química Geral, 12ª.ed., São Paulo: Saraiva, 2006.
http://www.joinville.udesc.br/portal/professores/franciscogm/materiais/Fun__es_org_nicas.pdf
http://web.ccead.puc-rio.br/condigital/mvsl/Sala%20de%20Leitura/conteudos/SL_funcoes_organicas.pdf
Texto originalmente publicado em https://www.infoescola.com/quimica/amidas/