As moléculas são espécies químicas eletricamente neutras constituídas por pelo menos dois átomos (de um mesmo elemento ou não). Sendo que, estes se unem por ligações estritamente covalentes (moleculares ou coordenadas); dessa forma, os compostos iônicos (ânion + cátion) não são formados por moléculas.
Exceto metais (Ferro, Níquel, Sódio...), gases nobres (Hélio, Argônio, Kriptônio...) e aglomerados iônicos (Cloreto de Sódio, Carbonato de Cálcio...), boa parte das outras substâncias são formadas por moléculas (Nitrogênio, Água, Açúcar, Ácidos hidrogenados...).
Durante uma ligação química, as eletrosferas de cada átomo ou íon encontram-se interagidas entre si e constituem uma nuvem eletrônica de aparência variável. Sendo esta aparência dependente da intensidade de atração de cada um sobre os elétrons.
A visível diferença entre as ligações iônicas e covalentes está justamente na distribuição da nuvem: nas moléculas-íon (formadas por ânions e cátions) a diferença de atração eletrônica é suficientemente grande para que a maior parte da nuvem se concentre em apenas um dos íons. Enquanto que nas moléculas, essa desigualdade de distribuição é menor (ou nula, se considerarmos as moléculas diatômicas de um mesmo elemento).

(Distribuição da nuvem eletrônica numa molécula-íon de NaCl. Onde a maior densidade é vista à direita – ao redor do átomo de Cloro.)
Ligações Covalentes
Como já mencionado, as moléculas são formadas por pelo menos dois átomos unidos através de uma ligação covalente (com compartilhamento de elétrons). Sendo esta dividida em dois tipos:
- Ligação covalente molecular – Neste tipo de ligação, pares eletrônicos são compartilhados e passam a fazer parte das duas eletrosferas simultaneamente. Assim, ambos atingem estabilidade eletrônica.
- Ligação covalente coordenada (ou dativa) – Geralmente, quando um átomo atinge o número de elétrons necessário para sua estabilidade eletrônica, não é possível realizar mais nenhuma ligação covalente molecular (exceto algumas moléculas que violam a regra do octeto). Entretanto, podem compartilhar pares de elétrons (como uma doação) a átomos de uma mesma molécula desde que continuem eletronicamente estáveis. Assim, os dois elétrons compartilhados provêem de um mesmo átomo.
Geometria Molecular
A disposição dos átomos numa molécula determina a sua geometria. Sendo esta intrinsecamente ligada à quantidade de pares eletrônicos ligantes e não-ligantes dos átomos constituintes.
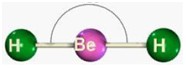
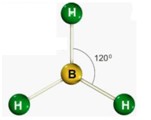
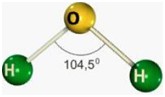
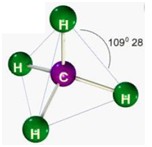
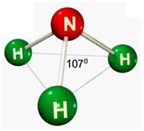
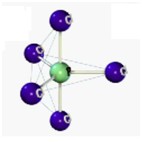
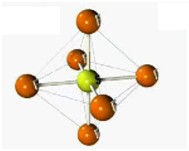
Dentre as possíveis geometrias, as mais comuns são: a linear, triangular, angular, tetraédrica, piramidal, bipiramidal e octaédrica.
| Geometria | Pares eletrônicos totais | Pares eletrônicos não ligantes | Pares eletrônicos ligantes |
| Linear | 2 5 6 |
0 3 4 |
2 2 2 |
| Triangular | 3 | 0 | 3 |
| Angular | 34 | 12 | 22 |
| Tetraédrica | 4 | 0 | 4 |
| Piramidal | 4 | 1 | 3 |
| Bipiramidal | 5 | 0 | 5 |
| Octaétrica | 6 | 0 | 6 |
Fontes:
SARDELLA, Antônio. Curso de química: Química geral, São Paulo – SP: Editora Ática, 2002. 25ª Edição, 2ª impressão. 448 págs.
Texto originalmente publicado em https://www.infoescola.com/quimica/molecula/