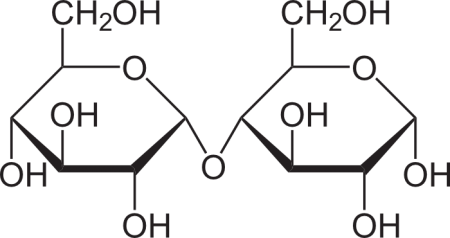
A Maltose (malte, do inglês clássico mealt, de origem germânica, e o sufixo '–ose') foi descrita pelo químico irlandês e químico Cornelius O’Sullivan, em 1872. É um carboidrato (glicídio ou açúcar), molécula orgânica formada por átomos de carbono, hidrogênio e oxigênio. A Maltose (α – D - glicopiranosil - (1→ 4) – D - glicopiranose) é um dissacarídeo, isto é, formada por duas moléculas de glicídios simples (glicose) unidas por uma ligação acetal. Essa ligação específica é denominada ligação α-l,4'-glicosídica. A ligação se dá entre C-1 de uma subunidade do açúcar e C-4 da outra.
Este açúcar não é encontrado livre na natureza, ele é obtido por processos de digestão, quando as enzimas que quebram as longas moléculas de amido em pedaços de maltose e, posteriormente, em duas moléculas de glicose, facilitando sua absorção pelo corpo. Possui sabor adocicado, no entanto, menos que a sacarose.
A maltose é o principal componente do malte, utilizado na fabricação da cerveja. Esta fabricação é um processo constituído por diversas etapas, onde ocorre a transformação química de carboidratos, como o milho, onde serão degradados, quebrados em glicídios de cadeias menores (maltose e glicose), ocorrendo a fermentação alcoólica por enzimas glicolíticas, presentes nas leveduras, como a Saccharomyces cerevisiae.
Maltose e a cerveja
Na formação do malte, as sementes dos cereais sofrem germinação com a síntese de enzimas responsáveis pela degradação dos polissacarídeos, chamada de malteação. Estes processos são bloqueados com o aumento controlado da temperatura. O malte contém α- e β-amilases, celulase, α-glicosidase e outras enzimas que catalisam a degradação dos polissacarídeos. Outra etapa da produção de cerveja é a mosturação, onde é preparado o meio nutriente para as leveduras. O malte será misturado com a água, permitindo a ação das enzimas hidrolíticas sobre a amilose, a amilopectina e a celulose, formando a maltose, a glicose e outros glicídios que são solúveis em água. E, para parar a degradação enzimática, o mosto líquido é fervido. Acontece o acréscimo do lúpulo, que dará sabor e aroma para a cerveja. Depois, leveduras são adicionadas ao mosto aerado e a fermentação alcoólica do mosto. Com isso, sem o açúcar não existiria a cerveja, já que ele é o alimento das leveduras, que transformam o mosto em cerveja.
Digestão da maltose
A digestão deste carboidrato tem seu início na boca, com ação da enzima chamada ptialina ou amilase salivar. Ela é secretada pelas glândulas salivares e atua na quebra dos carboidratos, mais especificamente a ligação alfa - 1→ 4 entre as moléculas de glicose do carboidrato, transformando-as em maltose e outros dissacarídeos ou oligossacarídeos. Em média, 30% do amido é digerido pela amilase salivar, sendo o restante digerido no intestino pela amilase pancreática e convertido em maltose. No entanto, o corpo ainda não consegue absorver este nutriente, que ainda está grande para absorção. Ele é encaminhado para o duodeno (uma parte do intestino delgado), onde a ptialina finaliza sua digestão, hidrolisando as ligações alfa 1 → 6. No duodeno as células intestinais secretam a enzima sacarase e isomaltase, que atuam na quebra até chegar aos monossacarrídeos, duas moléculas de glicose, podendo assim ser absorvidos pelo corpo.
Referências bibliográficas:
https://edisciplinas.usp.br/pluginfile.php/2234230/mod_resource/content/0/Resumo_06_Gr01.pdf
http://www2.iq.usp.br/docente/fgueiros/Carboidratos_alunos.pdf
http://www.ital.sp.gov.br/bj/artigos/bjft/2008/bjft_v11n4a37071.pdf
CURI, Roberto Abdallah. Produção de cerveja utilizando cevada como adjunto de malte. 2006. xi, 123 f. Tese (doutorado) - Universidade Estadual Paulista. Faculdade de Ciências Agronômicas de Botucatu., 2006. Disponível em: <http://hdl.handle.net/11449/101727>.
Texto originalmente publicado em https://www.infoescola.com/bioquimica/maltose/