A grande maioria dos metais já identificados possui propriedades físico-químicas bem semelhantes: facilidade em perder elétrons (frente ao seu ganho, em geral), elevados pontos de fusão e ebulição, boa condutividade elétrica e térmica, brilho característico.
Boa parte dessas propriedades são frutos da interação entre os átomos na rede cristalina que compõe o metal: observa-se que há um mesmo tipo de ligação entre átomos, que se repete ao longo da rede. Assim, é definida a ligação metálica.
O metal com maior ponto de fusão da tabela periódica é o tungstênio (PE = 3422°C), e isso é devido à interação dos átomos que o constitui: as forças de atração são tão intensas, que é necessária grande quantidade de energia para superá-las. Do mesmo modo, o ósmio é o elemento mais denso (d = 22,6), justamente pela forma de empacotamento que os cristais apresentam.
Aspectos da Ligação Metálica
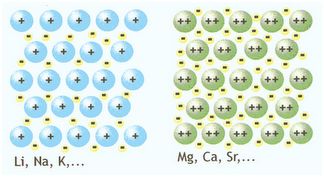 Os cátions de um metal encontram-se unidos por um “mar” de elétrons vizinhos: eles recobrem toda a superfície do metal, por isso corrente elétrica pode ser transmitida sem muita resistência.
Os cátions de um metal encontram-se unidos por um “mar” de elétrons vizinhos: eles recobrem toda a superfície do metal, por isso corrente elétrica pode ser transmitida sem muita resistência.
O sódio, por exemplo, apresenta íons Na+ lado a lado (com distância média praticamente constante) que permanecem submersos a uma camada de elétrons, quase que totalmente livres. Porque ainda que algumas literaturas considerem os elétrons de uma estrutura metálica livres, ainda será desprendida energia para ionizá-la; além disso, não pode ser deixado de lado o fato que a estrutura apresenta carga elétrica total nula e que, portanto, os elétrons não são totalmente externos aos átomos do retículo (mesmo que esse “mar” seja constituído por elétrons de valência – em constante movimento).
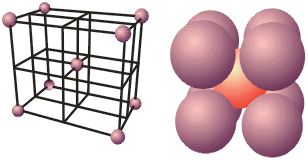
Assim como os outros sólidos, os metais são intimamente organizados por estruturas unitárias (células unitárias) que se repetem ao longo da cadeia.
Transmissão de calor e eletricidade
 Como já citado anteriormente, os elétrons de uma barra de cobre, por exemplo, possuem certa mobilidade. Assim, se for aplicado uma diferença de potencial em um dos lados dessa barra, certamente haverá condução de corrente elétrica. Assim como, se uma das pontas for aquecida, também haverá condução de calor (a outra ponta também aumentará de temperatura, gradativamente).
Como já citado anteriormente, os elétrons de uma barra de cobre, por exemplo, possuem certa mobilidade. Assim, se for aplicado uma diferença de potencial em um dos lados dessa barra, certamente haverá condução de corrente elétrica. Assim como, se uma das pontas for aquecida, também haverá condução de calor (a outra ponta também aumentará de temperatura, gradativamente).
Esses efeitos dão-se pela presença de tais elétrons circundantes aos cátions: ao aplicar uma tensão U, os elétrons tenderão a movimentar-se ordenadamente da região de maior potencial para a de menor potencial elétrico. Logo, uma corrente elétrica será detectada. Isso significa que quanto mais elétrons constituírem circundarem os cátions metálicos, corrente de maior intensidade será observada.
A transmissão de calor dá-se de também obedecendo a um gradiente de energia: ao aquecermos uma parte da barra, aumentamos a energia dos cátions mais próximos a fonte (já que começam a oscilar com mais intensidade); e, como os elétrons encontram-se móveis ao redor dos cátions internos, adquirem maior velocidade por se chocarem com estes. A partir daí, com a colisão contra outros cátions mais lentos (mais afastados da fonte) há transferência de parte dessa energia adquirida pela nova velocidade alcançada e, portanto, é verificada macroscopicamente a efetiva transmissão de calor.
Fontes:
ATKINS, Peter. LORETTA, Jones. Princípios de química: questionando a vida moderna e o meio ambiente; tradução Ricardo Bicca de Alencastro. – 3ª Ed. – Porto Alegre: Bookman, 2006. 968 páginas.
Texto originalmente publicado em https://www.infoescola.com/quimica/ligacao-metalica/