As características imprescindíveis a todo bom combustível é sua capacidade de decompor-se em um curto intervalo de tempo, em um processo exotérmico, isto é, que irá liberar enorme quantidade de energia. Neste aspecto, um dos mais famosos explosivos é nitroglicerina. Particularmente associada ao poder de detonação da nitroglicerina está a sua alta velocidade de decomposição. Assim, esta rápida decomposição irá liberar uma grande quantidade (volume) de gases em um tempo muito curto, o que acarretará em uma onda de choque supersônica. Apenas 800 gramas desse composto poderão produzir mais de 800 litros de gases após a detonação.
A maioria dos compostos apresenta em sua estrutura um ou mais átomos de nitrogênio, uma vez que sua molécula, quando submetida às condições adequadas, irá liberá-lo, na forma de nitrogênio gasoso, liberando assim grande quantidade de energia no balanço entre a quebra da ligação entre o nitrogênio e a molécula original e a formação da ligação tripla entre os átomos de nitrogênio existentes na molécula de gás nitrogênio (N2).
No caso da nitroglicerina, estão presentes os grupos nítricos -NO2, os quais tornam a molécula altamente instável e exotérmica, uma vez que a sua decomposição irá produzir moléculas de gás nitrogênio, muito mais estáveis do que as originais. Dessa forma, uma marca importante de um explosivo é a presença de nitrogênio, sobretudo na forma (-NO2) em sua molécula.
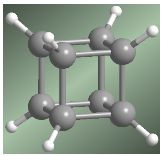
Uma molécula já sintetizada, mas muito intrigante, é o cubano, mostrada na Figura 1. Sua fórmula molecular é C8H8; trata-se de um hidrocarboneto cúbico com ângulos de ligação tensionados de 90o, os quais estão consideravelmente distantes daqueles para carbonos de hibridização sp3 (que apenas realizam ligações simples). Embora fora dos padrões teóricos, a molécula de cubano já foi sintetizada, apesar de apresentar grande instabilidade. Inclusive esta molécula é hoje comercializada por um alto valor.
As ligações tensionadas existentes na molécula de cubano apresentam-se como altamente energéticas, o que confere instabilidade à sua estrutura. O que se poderia imaginar ao nitrar-se a molécula? Por exemplo, até chegarmos a uma molécula de octanitrocubano? Esta molécula, um cubano nitrado em todos os seus átomos de carbono, possuiria a instabilidade inerente aos compostos de nitrogênio, além daquela oriunda do anel tensionado. Poderia ser então considerado o mais instável explosivo do mercado, e por isso mais energético. Talvez seja apenas uma questão de tempo, pois moléculas com maior número de carbonos tensionados já foram sintetizadas, e essa prática se torna cada vez mais comum nos meios acadêmicos.
Referências:
1. http://www.quimicaorganica.org/component/content/article/30/89-sintesis-organica.html
Texto originalmente publicado em https://www.infoescola.com/quimica/octanitrocubano/