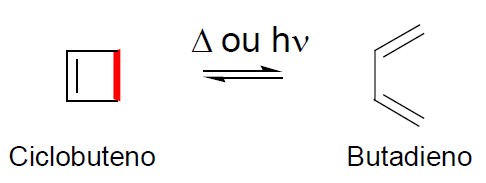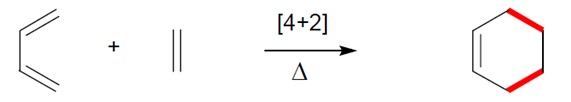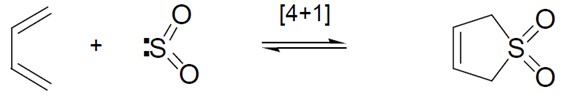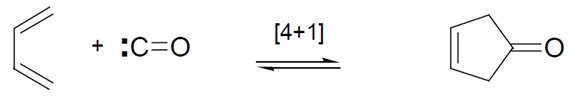As reações pericíclicas são aquelas nas quais algumas das moléculas envolvidas (ou todas, caso a reação possua apenas um reagente sob ação de energia) sofrem transformação estrutural pela reorganização contínua de elétrons, assim, estados de transição cíclicos são obtidos onde os orbitais participantes dos componentes mantêm uma interação ligante durante o decorrer da reação. São ditas “concertadas” por não haver estados intermediários, apenas a forma de cadeia aberta e fechada (embora haja casos em que compostos intermediários possam ser formados).
Constituem reações pericíclicas as reações eletrocíclicas (onde moléculas de cadeia aberta, sob radiação/calor, fecham em forma de anel pela formação de uma ligação sigma através de duas pi conjugadas); sigmatrópicas (com a mudança de posição de uma ligação sigma e rearranjo de outras pi); de cicloadição (através de uma ligação sigma formada por duas pi independentes entre si), dentre outras.
Alguns exemplos de reações pericíclias:
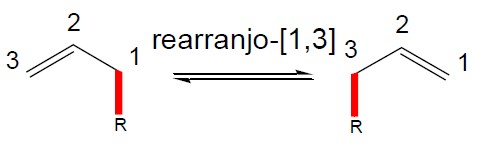
Sigmatrópica:
Reações de Cicloadição
Nas reações de cicloadição, dois sistemas pi (geralmente menores e independentes entre si, mesmo que estejam na mesma molécula) unem-se e formam uma ligação sigma. São descritas como reações [m+n], onde uma molécula de m átomos conjugados combina-se a uma de n átomos conjugados, exemplos:
Reação de Paterno-Büchi (cicloadição 2+2)
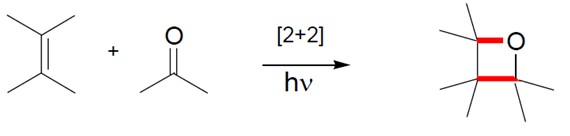 Reação de Diels-Alder (cicloadição 4+2)
Reação de Diels-Alder (cicloadição 4+2)
Observe que em ambas as reações há envolvimento de energia (sob forma de radiação apenas, ou calor – radiação no espectro do infra-vermelho), e um aduto é formado (ou seja, moléculas combinam-se e mantém, cada uma, a mesma estrutura caso estivessem separadas).
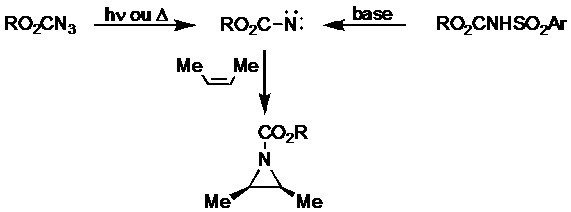
Caso a cicloadição se processe pela formação, ou clivagem (retroadição), de ligação sigma em um único átomo, a mesma recebe o nome de queletrópica. Nesse caso, o átomo doa e aceita, simultaneamente, um par de elétrons formando duas novas ligações, exemplo:
Estes processos queletrópicos podem dar origem a anéis de três ou cinco membros (uma vez que os estados de transição podem envolver quatro ou seis elétrons): a adição de nitrenos a alquenos e de carbenos (moléculas de carbono não hibridizado, ou seja, com apenas dois elétrons compartilhados) a ligações múltiplas contendo heteroátomos formam anéis de três membros (I) (as aziridinas – heterociclos hidrogenados); ao ponto que a reação apresentada acima (um butadieno com dióxido de enxofre) produz um anel de cinco membros (II), assim como a reação descrita abaixo entre butadieno e monóxido de carbono:
Fontes:
http://www.ufsm.br/quimica_organica/TOM-3.pdf
https://woc.uc.pt/quimica/getFile.do?tipo=2&id=650
http://sec.sbq.org.br/cd29ra/resumos/T0043-1.pdf
Texto originalmente publicado em https://www.infoescola.com/reacoes-quimicas/cicloadicao/