O elemento de transição cobre é um metal de coloração vermelha discretamente amarelada, com um brilho levemente opaco de aspecto agradável, está localizado no grupo I-B da tabela periódica, possui número atômico 29, massa atômica 63,55 g mol-, ponto de fusão de 1038°C, ponto de ebulição 2927ºC, é um metal macio, maleável e dúctil. O símbolo químico do metal é Cu, originado do latim “cuprum”, em alusão ilha do Chipre onde se acredita ter sido encontrado pela primeira vez.
É encontrado na natureza na forma de calcopirita CuFeS2, principalmente, existem outros, porém este apresenta um teor mais alto do metal, além de ser um dos metais que podem ser encontrados em estado elementar.
Este é um dos metais mais antigos de que se tem conhecimento, em virtude da idade do bronze no período neolítico, onde o cobre passou a ser muito utilizado, pesquisadores afirmam que a mineração do cobre tenha se iniciado há cerca de 5.000 anos. Houve um tempo que o metal foi considerado raro e seu custo bastante elevado, depois que este começou a ser encontrado com frequência e seu custo diminuiu, até o momento em que se descobriu a sua extrema propriedade de conduzir calor e energia elétrica, e seu uso tornar-se industrial, o valor aumentou consideravelmente, mas nada comparado ao ouro ou prata, apesar de ser considerado um metal nobre.
Em contato com ar atmosférico por tempo prolongado o cobre sofre oxidação formando em sua superfície uma película tóxica oriunda de uma mistura de óxidos, hidróxidos e carbonatos, de cor verde comumente chamada de azinhavre.A utilização do cobre é bastante ampla sendo difundida em vários segmentos industriais.
Entre eles temos:
- Utensílios de cozinha: tachos ciganos, panelas, bacias, talheres.
- Condutores elétricos: cabos de alta e baixa tensão, conectores, contatos elétricos em geral, fabricação de motores.
- Equipamentos: aquecedores solares, condutores de calor, tubulações de água.
- Ligas Metálicas: cobre e estanho forma o bronze, cobre e zinco forma o latão e por fim cobre e ouro forma o ouro 18 quilates,por exemplo, estas são as ligas mais comuns e utilizadas mas existem inúmeras outras.
Informações Importantes sobre o Cobre
Quimicamente falando do cobre, ele forma diversos compostos sendo o principal o sulfato de cobre CuSO4· 5H2O, utilizado como algicida e agente conferidor de coloração azul para água de piscinas, esse sal em estado anidro é de coloração branca, porém, em contato com o ar da atmosfera absorve a água e adquire coloração por ser higroscópico. A purificação do metal pode ocorrer de duas formas através do aquecimento dos minérios em que ele se encontra ou ainda após o aquecimento, passar por eletrólise para a obtenção de um maior grau de pureza. O cobre apresenta dois estados de oxidação Cu+ e Cu+2.
Na análise qualitativa esse elemento pode ser identificado facilmente, com a adição de solução de hidróxido de sódio formando um precipitado gelatinoso de cor azul intensa, é importante também salientar que para análise qualitaiva somente Cu+2, tem importância. O metal pertence ao segundo grupo de cátions, e apresenta um potencial de eletrodo padrão positivo de 0,34 Volts, o que impossibilita que sofra ataque de ácidos diluídos (HNO3, H2SO4 e HCl), porém é atacado e dissolve-se em água- régia, além de se dissolver com facilidade em H2SO4 concentrado a quente.
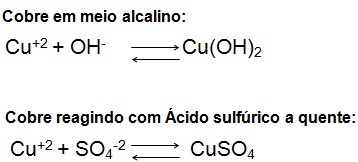
A reação do cobre em meio alcalino e com ácido sulfúrico:
Além de formar os compostos acima mostrados através das reações, forma também compostos de coordenação, ou seja, forma íons complexos com amônio e com a água tais como:
Tetraaminocuprato(II): [Cu(NH3)4]+2
Tetraaquocuprato(II): [Cu(H2O)4]+2 (este complexo é resultado da hidratação do íon cobre, e responsável pela coloração azul intensa da solução.)
Bibliografia:
Russel, J. B. Química geral. São Paulo: Makron Books, 2004.
Vogel, Arthur Israel, 1905-Química Analítica Qualitativa / Arthur I. Vogel ; [tradução por Antonio Gimeno da] 5. ed. rev. por G. Svehla.- São Paulo : Mestre Jou, 1981 .
Mahan, B. M. Química: um curso universitário. 4a ed. São Paulo: Edgard Blücher, 2003.
SHRIVER, DUWARD; ATKINS, PETER. Química inorgânica - 4ª edição. Porto Alegre, Bookman, 2008.
LEE, J.D.. Química inorgânica não tão concisa – tradução da 4ª edição inglesa. São Paulo, Edgard Blücher, 1996.
https://web.archive.org/web/20110512021709/http://www.ulbra.br:80/mineralogia/colecao/cobre_nativo.htm
Texto originalmente publicado em https://www.infoescola.com/elementos-quimicos/cobre/