Com o advento da radioatividade, questionamentos surgiram aos cientistas do início do século XX. A radioatividade não parecia obedecer aos pressupostos do modelo atômico de Thomson, pois aparentemente ela conseguia desintegrar o núcleo atômico, emitir radiações de vários tipos com a capacidade de atravessarem objetos. E foram estas radiações, mais especificamente a radiação alfa (que se assemelha a um átomo de hélio), que permitiu a Ernest Rutherford (1871 - 1937) realizar, juntamente com seus colaboradores, descobertas relativas ao átomo.
Rutherford apresentou ao mundo as conclusões de seu trabalho, indicando que algumas ideias de Thomson (herdadas do modelo de Dalton), encontravam-se inconclusivas frente ao novo fenômeno. Buscando elucidar questões importantes, Rutherford e seus colaboradores, Ernest Marsden e Johannes Wilhelm Geiger realizaram um experimento com emissões alfa, uma fina folha de ouro e o material fluorescente sulfeto de zinco (cuja função era a de detectar as emissões), conforme a figura a seguir:
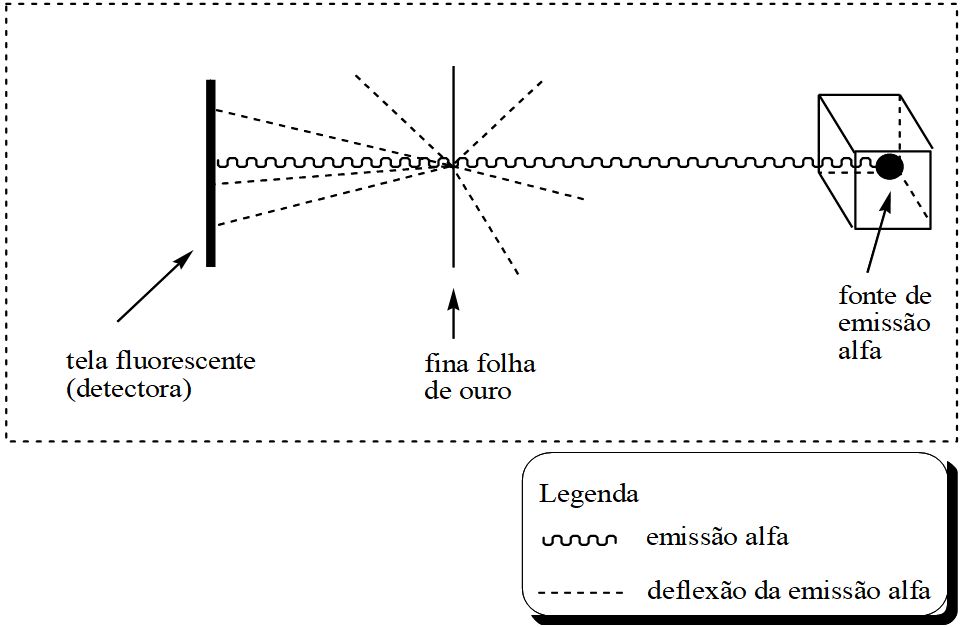
Esquema do experimento realizado por Rutherford e colaboradores.
Em seu experimento, Rutherford fez radiação alfa fosse emitida de maneira linear, objetivando que a radiação atingisse a finíssima folha de ouro em um único ponto. Utilizou um anteparo de sulfeto de zinco de modo a detectar as emissões defletidas (desviadas).
Pela teoria de Thomson, ao passar pela fina folha de ouro todas as emissões alfa apresentariam comportamento semelhante nos esperados desvios de seu caminho, devido ao fato do modelo de Thomson afirmar ter o átomo a forma de uma esfera maciça (sem espaços). O que Rutherford encontrou ia contra esta concepção, pois os desvios se mostraram raros (99% das emissões “transpassava” a folha de ouro sem sofrer desvio algum, desviando-se somente 1% das emissões).
Rutherford descartou a natureza maciça do átomo, intuindo sobre um novo modelo, onde o núcleo seria muito pequeno e muito mais denso que a periferia do átomo. O núcleo, formado por cargas positivas, desviaria as partículas alfa que interagissem com ele, e como se comprovou o núcleo ser bastante diminuto (em relação à recém-descoberta eletrosfera), isso explicaria o baixíssimo número de deflexões (1%).
Rutherford propôs então que o átomo seria composto de um núcleo pequeno e denso, sendo circundado por uma eletrosfera repleta de elétrons. Como os elétrons possuem massa quase desprezível, tal fato explicaria o seu nulo poder de deflexão das partículas alfa. A analogia em escala de grandeza que mais se aproxima é a do átomo é a de uma bolinha de gude (núcleo) colocada no meio de um grande estádio de futebol. Toda a área externa à bola de gude seria a eletrosfera.
Estava instaurado o modelo atômico de Rutherford, que ficaria conhecido na história da ciência como o modelo planetário do átomo. Na figura abaixo temos uma possível representação deste modelo.
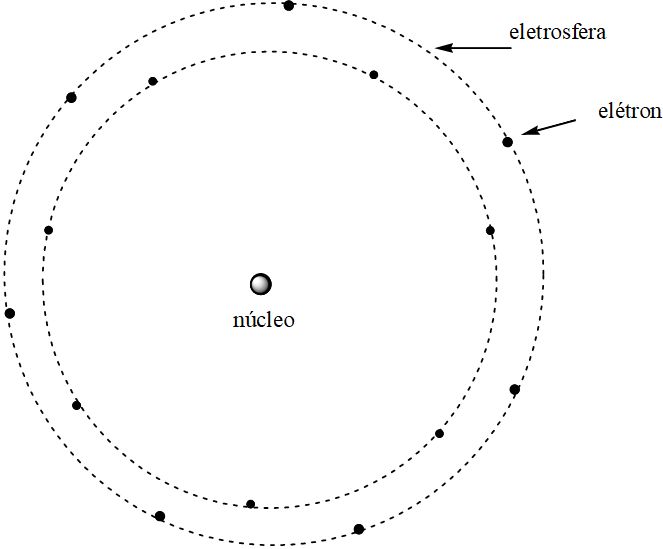
Representação sem escala do modelo atômico de Rutherford.
Rutherford afirmou que junto aos prótons, no núcleo, estariam presentes outras partículas atômicas, o nêutron, descoberto por James Chadwick em 1932.
Embora tenha explicado questões importantes da composição do átomo, o modelo de Rutherford não conseguia explicar porque o elétron não perde energia e “colide” com o núcleo ao se movimentar em órbita do mesmo, uma vez que na Física a atração de cargas elétricas de sinais opostos já era conhecida. A resposta para este enigma surgiu do estudo dos espectros da luz, inaugurando um novo capítulo: o modelo atômico de Rutherford-Bohr.
Referências:
LISBOA, J. C. F. Química, 1º ano: ensino médio. 1ª Ed. – São Paulo: Edições SM, 2010. (coleção Ser protagonista). p. 117 – 121.
FELTRE, R; YOSHINAGA, S. Atomística – 1ª Ed. – São Paulo: Moderna, 1970. p. 123 – 125.
FELTRE, R. Química Geral – 5ª Ed. – São Paulo: Moderna, 2000. p.87 – 90.
Texto originalmente publicado em https://www.infoescola.com/quimica/modelo-atomico-de-rutherford/