Aminas são compostos orgânicos derivados da amônia pela substituição de um, dois ou três de seus hidrogênios por radicais derivados dos hidrocarbonetos. Apresentam como fórmula geral R – NH2, RR’ – NH ou RR’R” – N. Na decomposição de plantas e animais liberam-se aminas; um exemplo é o cheiro de peixe podre observado na decomposição dos animais, onde esta função orgânica prevalece.
São utilizados em diversos meios industriais, no preparo de produtos sintéticos, como, por exemplo, medicamentos; como aceleradores no processo de vulcanização da borracha e as aromáticas na produção de corantes orgânicos. Além disso, apresentam também uma vasta variabilidade de funções no laboratório de síntese e identificação.
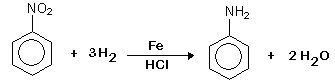
A anilina é a amina mais importante. É também denominada fenilamina; é obtida por hidrogenação do nitrobenzeno (por redução). Essa equação está mostrada na figura abaixo.
Nessa reação, um mol de nitrobenzeno reduz-se pela presença de três mols de hidrogênio gasoso, produzindo um mol de anilina e liberando dois mols de água. O processo somente é possível quando em meio ácido e catalisado por ferro.
A anilina é um liquido incolor, oleoso, pouco solúvel em água. Apresenta reações de substituição no núcleo aromático. O grupo – NH2 é orto e para dirigente e ativa estas posições no anel. Possui aplicação na síntese de corantes e medicamentos.
A metilamina, a dimetilamina e a trimetilamina são gases. As seguintes, até dez átomos de carbono, são líquidas e as demais são sólidas. As aminas de baixa massa molecular são solúveis em água. Nota-se, portanto, que para a função amina a hidrosolubilidade é inversamente proporcional ao peso molecular.
Os pontos de fusão e ebulição são mais elevados do que os compostos moleculares de mesmo peso molecular, mas, mais baixos do que os álcoois, ácidos carboxílicos e amidas.
As aminas possuem caráter básico. Ao reagirem com ácidos formam sal, segundo equação geral:
Uma importante aplicação laboratorial das aminas aromáticas, como a anilina, é a diazotação. Desse modo, pode-se identificar um grupo NH2 ligado ao anel aromático através de uma reação de diazotação. Esta reação é válida para qualquer amina aromática. Formam-se como produtos sais de diazônio, que são pontos de partida para a síntese de muitos compostos orgânicos, como, por exemplo, os fenóis. Ocorrem somente em temperatura inferior a 0°C, pois estes sais sofrem decomposição pelo calor. Um composto de diazônio, quando sintetizado, caracteriza-se por apresentar uma coloração amarelo-claro, independentemente a amina de partida.
Referências:
SARDELLA, Antônio; MATEUS, Edegar; Curso de Química: química geral, Ed. Ática, São Paulo/SP – 1995.
MAHAN, Bruce M.; MYERS, Rollie J.; Química: um curso universitário, Ed. Edgard Blucher LTDA, São Paulo/SP – 2002.
Texto originalmente publicado em https://www.infoescola.com/fisica/propriedades-fisicas-das-aminas/