A adição oxidativa, em química organometálica, refere-se à reação entre um complexo metálico orgânico (formado por pelo menos um átomo metálico ou metalóide com uma ou mais ligações com átomos de carbono ou radicais orgânicos) e outra molécula ou composto, onde o mesmo sofre redução. Assim, o complexo é oxidado (doa elétrons para a outra espécie).
Esse tipo de reação é observado quando insere-se uma molécula X-Y no complexo (com sítios de coordenação vagos). Com isso, o metal central sofre acréscimo de duas unidades no estado de oxidação formal, pois há rompimento da ligação X-Y, e ambos estabilizam-se “retirando” elétrons do metal.
São mais comuns em metais de configuração eletrônica d8 (Rh(I), Ir(I), Co(I), Pd(II), Pt(II)), ou d10 (Pd(0), Pt(0)). E, se o complexo já tiver atingido o número 18 em elétrons ligantes totais (obedecendo, portanto, a regra do octeto), a adição ocorrerá com a expulsão de alguns dos ligantes. A não ser quando complexo foge a essa regra.
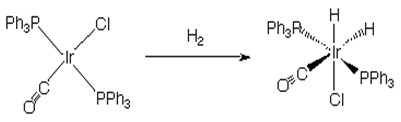
A reação abaixo mostra a adição oxidativa de hidrogênio molecular (H-H) ao complexo IrCl(CO)(PPh3)2, sendo PPh3 a trifenilfosfina (ou simplesmente fosfina):
Apesar de a forma trans (com ligantes de maior massa molecular em lados opostos no arranjo geométrico) ser geralmente preservada, nesse exemplo, nem sempre isso ocorre, e isômeros cis-trans podem ser obtidos.
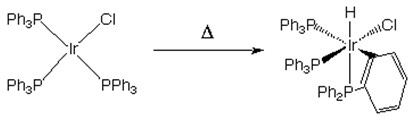
Há ainda, possibilidade da adição oxidativa ser intramolecular. Ou seja, através de uma perturbação na molécula (com fornecimento de energia), os ligantes podem se reorganizar (com quebra de ligações ou não) e provocarem elevação do estado de oxidação formal do metal.
Por exemplo, o aquecimento do IrCl(PPh3)3 rompe a ligação entre hidrogênio e o anel benzênico de um dos radicais trifenilfosfina. Como consequência, ambos unem-se ao Irídio.
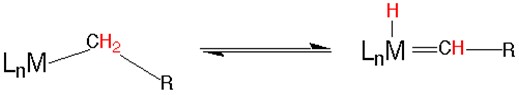
 O fenômeno contrário é a eliminação redutiva, onde o átomo metálico sofre diminuição do seu estado de oxidação (sofrendo redução) pela saída dos átomos X e Y, gerando a molécula de origem XY, ou ainda, ambos podem se rearranjar de modo a continuarem no complexo:
O fenômeno contrário é a eliminação redutiva, onde o átomo metálico sofre diminuição do seu estado de oxidação (sofrendo redução) pela saída dos átomos X e Y, gerando a molécula de origem XY, ou ainda, ambos podem se rearranjar de modo a continuarem no complexo:
O exemplo acima mostra as respectivas formas mais reduzida e oxidada do metal M convivendo em equilíbrio dinâmico (ambos os isômeros podem existir ao mesmo tempo).
O hidrogênio migrante pode ser classificado de acordo com a sua posição na cadeia, portanto no último exemplo, há eliminação redutiva intramolecular de um hidrogênio α:
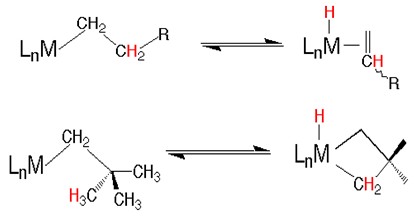
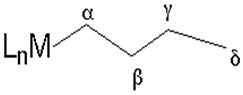 Seguem os exemplos genéricos de eliminação redutiva intramolecular envolvendo hidrogênios β e γ:
Seguem os exemplos genéricos de eliminação redutiva intramolecular envolvendo hidrogênios β e γ:
Fontes:
http://goldbook.iupac.org/O04367.html
https://woc.uc.pt/quimica/getFile.do?tipo=2&id=577
Texto originalmente publicado em https://www.infoescola.com/quimica/adicao-oxidativa/