O iodofórmio possui fórmula molecular CHI3; trata-se de uma substância que ainda hoje é utilizada como antisséptico nos hospitais, e apresenta grande importância na odontologia. Apresenta-se sob a forma de cristais de coloração amarelo-pálido e brilhantes. Possui efeito semelhante ao clorofórmio, mas com ação de átomos de iodo.
O iodofórmio é um medicamento empregado como anti-séptico e agente antiinfeccioso de uso tópico. Tem uso veterinário como anti-séptico e como desinfetante para lesões superficiais.
O IODOFÓRMIO apresenta as seguintes propriedades:
- Provoca uma ação local sobre os tecidos, diminuindo a secreção e a exsudação;
- Estimula a proliferação celular;
- Tem leve poder antisséptico, porém de ação prolongada;
- Decompõe-se lentamente à temperatura corporal e ativa a fagocitose de resíduos irritantes aos tecidos;
- É intensamente radiopaco.”1
Este texto propõe a realização em laboratório da síntese deste medicamento, o iodofórmio, sob variação de um reagente por síntese.
A tintura de iodo é uma solução aquosa onde se tem o equilíbrio, no qual o elemento químico iodo apresenta variação de número de oxidação, de 1 a 3 nenativos.
I-(aq) + I2(aq) ↔ I3-(aq)
Ao se tratar a acetona (CH3COCH3) ou o etanol (CH3CH2OH) com tintura de iodo, na presença de solução aquosa de hidróxido de sódio (NaOH), ocorre a formação do iodofórmio (CHI3), um sólido amarelo-claro insolúvel em água, conforme mostram as equações representadas na Figura 1. Este sólido é o iodofórmio, o qual pode ser identificado pelo seu forte odor característico.
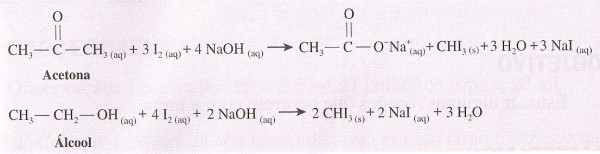
Figura 1. Síntese do iodofórmio a partir de diferentes funções orgânicas.
Pode-se ver nas equações que o iodofórmio pode ser obtido a partir da acetona e também a partir do álcool, duas funções distintas da química orgânica. Verifica-se, entretanto, que a formação de subprodutos é menor na segunda síntese, o que demonstra um maior rendimento de reação.
● PROCEDIMENTO EXPERIMENTAL:
- Colocar 50mL de água e 2,5mL de NaOH 3M em um copo de béquer. Homogeneizar e adicionar 5mL de acetona. Agitando, adicionar 10 gotas de tintura de iodo. Agitar a mistura e observar durante 5 minutos.
- Colocar 50mL de água e 2,5mL de HaOH 3M em um copo de béquer. Homogeneizar e adicionar 2,5mL de etanol. Agitando, adicionar 40 gotas de tintura de iodo. Agitar a mistura e observar durante 10 minutos.
- Caso necessário, trabalhar com NaOH sólido (20g).
- Utilizando um papel filtro previamente pesado, filtrar os produtos obtidos e pesá-los. Calcular o rendimento conforme massa dos solventes utilizada.
- Armazená-los em frascos distintos conforme o solvente utilizado.
Referências:
1. http://www.biodinamica.com.br/produtos
PERUZZO, Francisco Miragaia (Tito); CANTO, Eduardo Leite; Química na Abordagem do Cotidiano, Ed. Moderna, vol.1, São Paulo/SP- 1998.
RUSSELL, John B.; Química Geral vol.1, São Paulo: Pearson Education do Brasil, Makron Books, 1994.
Texto originalmente publicado em https://www.infoescola.com/quimica/sintese-organica-do-iodoformio/