A química pode ser dividida em seis áreas do conhecimento: química geral e inorgânica (estuda os compostos inorgânicos e a estrutura da matéria), química orgânica (estuda os compostos de carbono, suas reações e propriedades), química analítica (estuda técnicas de identificação e quantificação de substâncias químicas), físico-química (estuda os aspectos termodinâmicos e cinéticos das substâncias e reações) e bioquímica (estuda a interação das substâncias químicas com organismos vivos).
A primeira utilização de compostos orgânicos pelo homem foi na descoberta do fogo; quase tudo que sofre combustão é um composto orgânico. Em resumo, toda a vida é baseada no carbono, desde o combustível que queimamos, até a constituição do nosso próprio corpo. Cerca de 60% da massa corpórea de um indivíduo é de compostos orgânicos (desconsiderando-se a água). A diversidade dos compostos orgânicos existentes também é grande, cerca de 20 milhões, entre naturais e sintéticos.
Entre o final do século XVIII e início do século XIX os cientistas começaram a dedicar tempo para entender a química dos organismos vivos, isolando e identificando substâncias presentes nos corpos. Nessa época, acreditava-se na Teoria da Força Vital de Berzelius, que postulava que os compostos orgânicos só poderiam ser produzidos por organismos vivos, dai o termo ‘química orgânica’. Alguns anos mais tarde, em 1828, Friedrich Wöhler conseguiu sintetizar em laboratório a substância ureia a partir de um composto inorgânico, derrubando a Teoria de Berzelius. Hoje, a química orgânica é a área que estuda os compostos de carbono com propriedades características, suas diferentes funções, comportamento espacial e reações.
A química orgânica pode ser subdividida em:
Conteúdo deste artigo
Estudo do carbono
É a parte da química orgânica que estuda o elemento carbono, utilizando o conhecimento de ligações químicas para determinar os tipos de ligações possíveis para o elemento e sua hibridização em cada caso, bem como sua capacidade de encadeamento e seu comportamento dentro das moléculas orgânicas.
Nesta seção também estudamos a classificação das cadeias de carbono e os princípios básicos de nomenclatura de cadeias.
Abaixo temos um resumo da regra de nomenclatura de cadeias orgânicas.
Nomenclatura: PREFIXO + INFIXO + SUFIXO (depende da função orgânica)
| Sufixo | Infixo | ||
| N° de Carbonos | Saturação da Cadeia | ||
| 1C | MET | Saturadas | AN |
| 2C | ET | ||
| 3C | PROP | Insaturadas | |
| 4C | BUT | ||
| 5C | PENT | 1 dupla | EN |
| 6C | HEX | 2 duplas | DIEN |
| 7C | HEPT | 3 duplas | TRIEN |
| 8C | OCT | 1 tripla | IN |
| 9C | NON | 2 triplas | DIIN |
| 10C | DEC | 3 triplas | TRIIN |
| 11C | UNDEC | ||
Estudo das funções orgânicas
O estudo das funções orgânicas é a área onde aprende-se a identificar as funções, seus grupamentos funcionais e sua nomenclatura oficial.
A tabela abaixo apresenta as principais funções orgânicas e seus respectivos grupamentos funcionais.
| Função | Grupo Funcional |
| Hidrocarboneto | H, C |
| Álcool | ‒OH |
| Fenol | Ar‒OH Caromático |
| Éter | ‒O‒ |
| Aldeído | 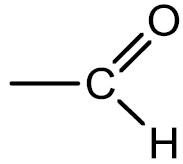 |
| Cetona | 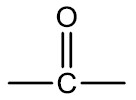 |
| Ácido carboxílico | 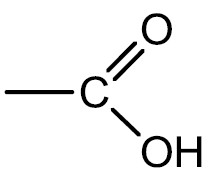 |
| Éster | 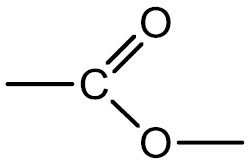 |
| Haleto orgânico | ‒X (F,Cl, Br, I) |
| Haleto de ácido | (F, Cl, Br, I) |
| Amina | ‒NH2 |
| Amida | 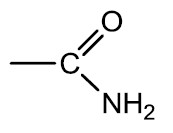 |
| Nitrocomposto | ‒NO2 |
| Nitrila | ‒CN |
| Ácido sulfônico | ‒SO3H |
| Composto de Grignard | ‒MgX (F, Cl, Br, I) |
Propriedades dos compostos orgânicos
Estuda as propriedades inerentes a cada classe de funções e como estas interagem entre si. Dentre as propriedades estudadas estão temperatura de fusão, temperatura de ebulição, solubilidade, acidez e basicidade.
Em geral, todas as propriedades físicas dependem das interações intermoleculares presentes nos compostos. Vale lembrar a ordem de força das interações intermoleculares: Ligação Hidrogênio > Dipolo-dipolo > Van der Waals.
Isomeria
A isomeria é o fenômeno onde duas ou mais substâncias diferentes apresentam a mesma fórmula molecular e possuem diferentes fórmulas estruturais. Este ramo da química estuda as semelhanças entre cadeias carbônicas e funções, bem como seu comportamento espacial. A isomeria é dividida em plana (considera apenas a fórmula estrutural plana) e espacial (considera a fórmula estrutural espacial e a simetria da molécula).
É um campo importante pois a isomeria está presente principalmente em medicamentos, onde muitas vezes temos isômeros ativos (aqueles que tem interesse farmacológico) e inativos.
Reações orgânicas
As reações orgânicas ocorrem tanto em processos orgânicos quanto industriais, sendo assim, é importante o seu estudo para entendermos a bioquímica, os processos metabólicos e interações que ocorrem nos seres vivos. É uma área de grande incentivo de pesquisa em laboratórios e universidades pois é a base do desenvolvimento de remédios, processos da indústria alimentícia, dentre outros.
As reações orgânicas são divididas em substituição, adição e eliminação.
Reações de substituição: É uma reação de dupla troca onde um átomo ou grupo de átomos é substituído.
Exemplo:
CH4 + Cl2 → CH3Cl + HCl
Reações de adição: é a reação onde dois ou mais reagentes se unem para formar um só produto. Ocorre geralmente em compostos insaturados ou cíclicos.
Exemplo:
H2C=CH2 + H2 → H3C‒CH3
Reações de eliminação: É o oposto da reação de adição. Neste caso, um único reagente sofre um processo onde a molécula é quebrada em duas ou mais moléculas menores. Geralmente ocorre com utilização de um catalisador ou calor.
Exemplo:
CH3‒CH3 → CH2=CH2 + H2
Polímeros
Polímeros são macromoléculas formadas após uma reação de polimerização entre monômeros. Existem polímeros naturais, como as proteínas, a celulose e o látex, e existem polímeros sintéticos, que são sintetizados em laboratório de forma a “copiar” os naturais. Exemplos de polímeros sintéticos são os plásticos, o isopor e o nylon.
Dentre os polímeros sintéticos temos dois tipos: polímeros de adição e de condensação.
Polímeros de adição: os monômeros utilizados na produção desses polímeros devem apresentar pelo menos uma dupla ligação entre carbonos. Durante a polimerização, ocorre a ruptura da ligação π e a formação de duas novas ligações simples.
Exemplos: PET, PVC, PVA e borrachas sintéticas.
Polímeros de condensação: são formados pela polimerização de dois monômeros diferentes, liberando uma molécula pequena (geralmente a água) durante a condensação. Não é necessário que haja dupla ligação em um dos monômeros, mas é preciso que os dois sejam de funções diferentes.
Exemplos: poliéster, silicone, fórmica (baquelite).
Bioquímica
Neste ramo da química orgânica estudamos com mais aprofundamento as moléculas responsáveis pela constituição e manutenção da vida dos seres vivos. Dentre as principais biomoléculas estão os carboidratos, as proteínas e os lipídios.
Carboidratos: são polissacarídeos (açúcares), como a glicose e a frutose. Tem como função principal a de fornecer energia ao nosso organismo.
Proteínas: são polímeros de condensação naturais formados de até 20 aminoácidos diferentes. Tem como função constituir fibras musculares, cabelo e pele. Algumas funcionam como catalisadores em reações do organismo, sendo chamadas de enzimas.
Lipídios: são formados a partir da reação de um ácido graxo com o glicerol. Os mais importantes são os óleos e as gorduras. O triglicerídeo é um lipídeo que possui três grupamentos éster na sua estrutura.
Petróleo
O petróleo possui em sua composição principalmente hidrocarbonetos e seus componentes são de grande importância econômica. Aproximadamente 85% dos materiais obtidos a partir do petróleo são usados como combustíveis e os outros 15% na indústria petroquímica, como por exemplo, na produção de plásticos e asfalto. Por ser um material de tamanha importância, o estudo de seu processo de refino e craqueamento é um dos ramos de estudo da química orgânica.
Bibliografia:
Atkins, P.W., Jones, L., Princípios de química: questionando a vida moderna e o meio ambiente 5ª ed., Porto Alegre: Ed. Bookman, 2012.
Usberco J., Salvador E., Química Geral, 12ª.ed., São Paulo: Saraiva, 2006.
Texto originalmente publicado em https://www.infoescola.com/quimica/quimica-organica/
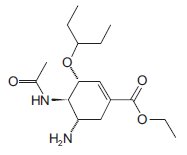 O oseltamivir, representado na figura ao lado, é o princípio ativo do antiviral Tamiflu® que é utilizado no tratamento da gripe A (H1N1). Assinale a opção que NÃO indica uma função orgânica presente na estrutura da molécula do oseltamivir.
O oseltamivir, representado na figura ao lado, é o princípio ativo do antiviral Tamiflu® que é utilizado no tratamento da gripe A (H1N1). Assinale a opção que NÃO indica uma função orgânica presente na estrutura da molécula do oseltamivir.