Os nitrocompostos são compostos orgânicos que apresentam como característica a presença em sua estrutura do grupo funcional nitro (NO2). Podem ser representados da seguinte forma:
R─NO2
Onde R pode ser um anel aromático (anel contendo 6 carbonos com ligações simples e duplas alternadas), ou uma cadeia alifática (cadeia carbônica aberta).
Os nitrocompostos são derivados do ácido nítrico (HNO3), onde esse reage com um grupo orgânico R. Durante a reação, o composto orgânico perde um átomo de hidrogênio formando um radical R, e o ácido perde a hidroxila, ocorrendo então à substituição desta pelo radical R, conforme esquema simplificado abaixo:
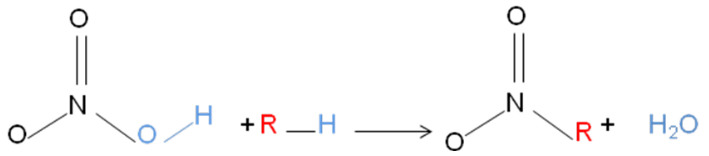
Figura 1: reação simplificada do ácido nítrico com um hidrocarboneto.
Esses compostos podem conter um ou mais grupos nitro em suas moléculas.
Em relação à nomenclatura, seguindo a regras da IUPAC (União Internacional de Química Pura e Aplicada) devemos seguir a sequencia:
Nitro + Nome do grupo orgânico R
Utilizando como exemplo o composto H3C__CH2__ CH2__NO2, vemos que ele é formado por um grupo nitro e um hidrocarboneto, representado pela cor vermelha. Lembrando rapidamente das regras de nomenclatura de compostos orgânicos, sabemos que uma cadeia com 3 carbonos, usa o prefixo prop, como as ligações entre o átomos de carbono é simples, usamos o infixo an, e como ele é um radical proveniente de um hidrocarboneto, temos como sufixo a terminação o, por isso o nome fica prop + na + o = propano. Com o grupo nitro está ligado ao primeiro átomo de carbono da cadeia, isso deve ficar bem claro no nome, dessa forma nitrocomposto acima é 1- nitropropano.
Caso o composto seja formado por mais de um grupo nitro como é o caso da molécula abaixo, devemos indicar a posição de todos os grupamentos. Dessa forma temos nesse caso o 2,4,6-trinitro-octano.
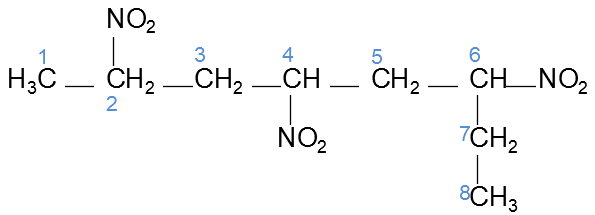
Figura 2: Estrutura do 2,4,6-trinitro-octano.
A mesma regra vale para os compostos aromáticos, então, por exemplo, no caso da molécula a seguir, constituída por um grupo nitro e um anel aromático (benzeno), o nome do composto fica nitrobenzeno.
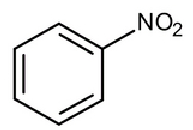
Figura 3: Nitrobenzeno.
O nitrobenzeno é bastante utilizado como solvente de substâncias orgânicas, e apresenta como características principais ser insolúvel em água e tóxico.
Em relação às propriedades físicas, de maneira geral a maioria dos nitrocompostos são encontrados na forma de líquido viscoso quando em temperatura ambiente. Porém, existem exceções, como é caso dos compostos de massa molar mais baixa, que são mais fluídos. São substâncias polares, insolúveis em água (com exceção do nitrometano e nitrobutano, que por apresentarem baixa massa molar, são pouco solúveis em água) e densos. Entre os alifáticos e aromáticos existem algumas diferenças marcantes como aroma agradável para os primeiros e desagradável para o segundo. Além disso apresentam diferentes aplicações.
Os nitrocompostos aromáticos são muito reativos, e por esse motivo são utilizados na fabricação de explosivos. Quanto mais grupos nitro estiverem presentes na sua estrutura, mais reativo, e consequentemente explosivos, são os nitrocompostos aromáticos. Como exemplos podemos citar o 2-metil-1,3,5-trinitro-benzeno ou 2,4,6-trinitrotolueno (TNT) e o 2,4,6 – dinitrotolueno (DNG). Temos também a trinitroglicerina (TNG), que além de poder ser utilizado como explosivo, também tem aplicação na medicina como vasodilatador coronário. Outras aplicações são na utilização de agrotóxicos, aditivos, corantes, fungicidas entre outros.
Referencias:
Tito e Canto. Química na Abordagem do Cotidiano. Volume único, parte C – Química Orgânica. Editora Saraiva 2005.
T. W. Graham Solomons. QUÍMICA. ORGÂNICA volume 1; Sétima edição. Editora LTC livros técnico e científicos, 2000.
T. W. Graham Solomons. QUÍMICA. ORGÂNICA volume 2; Sétima edição. Editora LTC livros técnico e científicos, 2000.
Texto originalmente publicado em https://www.infoescola.com/quimica/nitrocompostos/