As cetonas (função cetona) são compostos que apresentam o grupamento carbonila (C=O) no meio da cadeia, ou seja, em um carbono secundário. São formadas pela oxidação de álcoois secundários, onde um átomo de hidrogênio (ligado ao oxigênio) é retirado e o átomo de oxigênio passa a fazer uma ligação dupla com o carbono da cadeia. As cadeias desta classe de compostos podem ser tanto abertas quanto fechadas (aromáticas ou não).
Cadeias pequenas (até dez átomos e carbono) levam a cetonas no estado líquido, menos densas que a água, de cheiro agradável e que, em geral, são parcialmente solúveis – exceção para a propanona que é totalmente solúvel. Cadeias com mais de dez carbonos levam a cetonas sólidas e insolúveis em água.
Industrialmente, muitos dos óleos essenciais extraídos de flores e frutos e usados na produção de perfumes são compostos cetônicos. Elas também são usadas na extração de gorduras de sementes como o girassol e o amendoim. Cetonas também podem ser usadas para extrair cocaína das folhas de coca, o que torna seu uso restrito e fiscalizado por órgãos da polícia federal.
As cetonas com pelo menos um hidrogênio α (hidrogênio ligado no carbono vizinho ao grupo carbonila) encontram-se em um equilíbrio dinâmico com um isômero denominado enol. Esse equilíbrio é conhecido como tautomeria ceto-enólica.
Grupo Funcional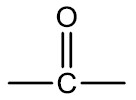
Nomenclatura das cetonas
Prefixo + tipo de ligação + ONA
| Propanona ou acetona |
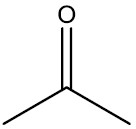 |
| 3-metil-pentan-2-ona |
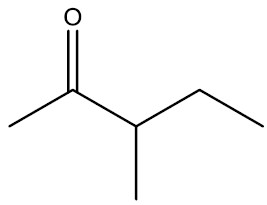 |
Quando há a presença de mais de um grupo carbonila na estrutura, pode-se utilizar os prefixos di, tri, tetra na nomenclatura:
| Hexan-2,4-diona |
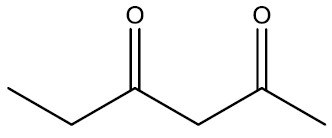 |
Existe uma nomenclatura usual em que o grupo carbonila é denominado cetona, e seus ligantes são considerados radicais.
| Dietil-cetona |
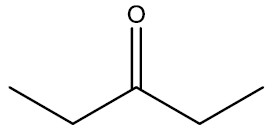 |
| Etil-propil-cetona |
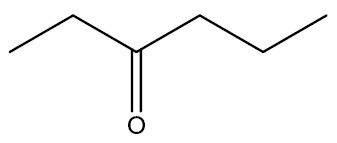 |
As cetonas podem ser obtidas em laboratório através de ozonólise de alcenos, hidratação de alcinos, método de Piria, síntese de Friedel-Crafts e mais comumente, pela oxidação de álcoois secundários.
Em geral, as cetonas são mais estáveis que seus enóis precursores e é possível obter 100% do produto cetônico quando os alcinos sofrem hidratação catalisada por ácido. O método-padrão de hidratação de alcinos utiliza o ácido sulfúrico aquoso como o meio reacional e usa o sulfato de mercúrio (II) ou o óxido de mercúrio (II) como um catalisador.
Algumas cetonas importantes
Acetona (propanona): é um líquido inflamável, incolor, com cheiro agradável e solúvel em água. A cetona mais simples é usada como solvente (de lacas, resinas, acetileno), na extração de óleos vegetais e na fabricação de medicamentos hipnóticos como o sulfonal (um sonífero).
Acetofenona: é a cetona aromática mais simples sendo incolor e de alta viscosidade. É utilizada como precursor na preparação de diversas resinas e fragrâncias (principalmente como aroma artificial de amêndoa, cereja, jasmim e morango), sendo também o precursor acadêmico clássico para o estireno.
Leia também:
Bibliografia:
Atkins, P.W., Jones, L., Princípios de química: questionando a vida moderna e o meio ambiente 5ª ed., Porto Alegre: Ed. Bookman, 2012.
Usberco J., Salvador E., Química Geral, 12ª.ed., São Paulo: Saraiva, 2006.
http://www.joinville.udesc.br/portal/professores/franciscogm/materiais/Fun__es_org_nicas.pdf
http://web.ccead.puc-rio.br/condigital/mvsl/Sala%20de%20Leitura/conteudos/SL_funcoes_organicas.pdf
Texto originalmente publicado em https://www.infoescola.com/quimica/cetonas/