Alcenos, alquenos ou olefinas são hidrocarbonetos que possuem cadeia aberta e ligações duplas C=C (ligação π). A presença da ligação dupla nos alcenos cíclicos e acíclicos lhes confere características químicas bem diferentes dos alcanos, tornando-os mais reativos.
O termo olefina significa oleoso, pois os alcenos, ao reagirem com halogênios, geram compostos de aspecto gorduroso, do latim oleum = óleo + affinis = afinidade.
Quimicamente falando, os alcenos são apolares e insolúveis em água. Em geral, os de cadeia normal de dois a quatro carbonos são gases, de cinco a dezesseis carbonos são líquidos e de dezessete carbonos em diante são sólidos, na temperatura ambiente.
Enquanto os alcanos são muito comuns na natureza, os alcenos em geral são sintéticos. Apenas alguns são possíveis de se obter a partir do craqueamento do petróleo, como é o caso do eteno. Industrialmente é possível obter alcenos através da pirólise de alcanos.
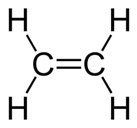
Eteno.
- Grupo Funcional: C, H.
- Nomenclatura: regra geral IUPAC + terminação -ENO
- Fórmula Geral: CnH2n
Conteúdo deste artigo
Nomenclatura dos alcenos
Na nomenclatura dos alcenos, é importante que a contagem da cadeia principal comece na extremidade mais próxima da dupla ligação. A posição da dupla deve vir antes do infixo que indica o tipo de ligação. Em alcenos com mais de uma ligação dupla, é importante utilizar a menor numeração para as insaturações, para evitar ambiguidade entre estruturas.
Exemplos:
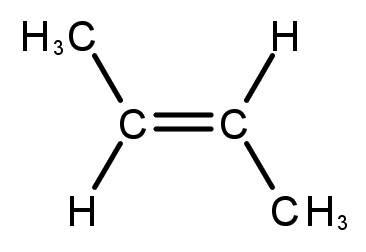 |
But-2-eno |
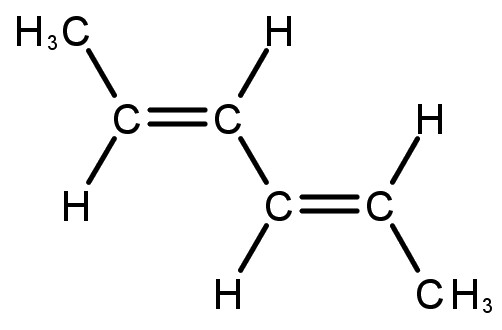 |
Hex-2,4-dieno |
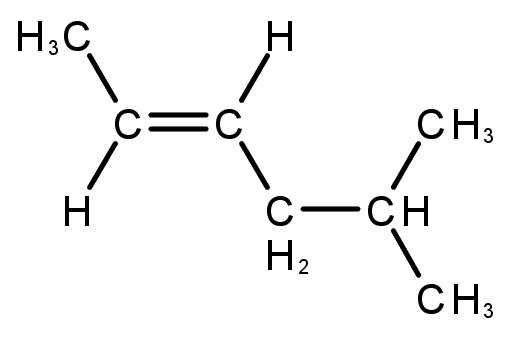 |
5-metil-hex-2-eno |
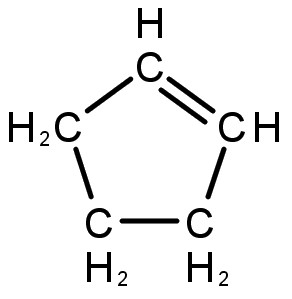 |
ciclopenteno |
É muito frequente que alcenos apresentem isomeria geométrica (cis-trans) devido a possibilidade de se traçar um plano de simetria sobre a ligação dupla da molécula. Essa propriedade amplia os possíveis campos de utilização dessa classe de compostos.
Alguns alcenos importantes:
Eteno ou etileno
O etileno é utilizado comercialmente e industrialmente para diversos fins, dentre eles:
- Anestésico: o etileno é um anestésico moderado.
- Amadurecimento de frutas: é utilizado para o amadurecimento artificial de frutas após colheita. É mais fácil colher as frutas verdes para transporte e adicionar o etileno nos depósitos para amadurecê-las artificialmente.
- Matéria prima para polímeros: o etileno é uma importante matéria prima na fabricação de polímeros e plásticos como o polietileno e o policloreto de vinila (PVC).
- Obtenção de álcool: em países com pouco espaço para agricultura, o etileno é utilizado como matéria prima na fabricação de álcool etílico (etanol).
Propeno ou propileno
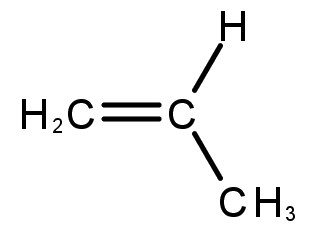
Propeno.
O propileno é a maior matéria-prima da indústria petroquímica, sendo utilizado em larga escala na indústria de polímeros. Seus usos incluem:
- Obtenção do polipropileno: um polímero muito usado nas indústrias têxteis e na produção de utensílios domésticos, dentre outras aplicações.
- Combustível industrial: devido a sua chama ser mais quente que o propano, ele é mais utilizado como combustível.
- Produção de ácido acrílico: processo realizado a partir da oxidação parcial catalítica do propileno.
Radicais dos Alcenos
Os radicais dos Alcenos são formados pela presença de um ou mais elétrons livres. Recebem a terminação -enil no lugar de –eno. Exemplos:
| Número de carbonos | Prefixo | Molécula | Radical | Nomenclatura |
| 2 | Et | C2H4 | C2H3 | Etenil ou vinil |
| 3 | Prop | C3H6 | C3H5 | Propenil ou alil |
| 4 | But | C4H8 | C4H7 | Butenil |
| 5 | Pent | C5H10 | C5H9 | Pentenil |
Bibliografia:
Atkins, P.W., Jones, L., Princípios de química: questionando a vida moderna e o meio ambiente 5ª ed., Porto Alegre: Ed. Bookman, 2012.
Usberco J., Salvador E., Química Geral, 12ª.ed., São Paulo: Saraiva, 2006.
http://www.joinville.udesc.br/portal/professores/franciscogm/materiais/Fun__es_org_nicas.pdf
http://web.ccead.puc-rio.br/condigital/mvsl/Sala%20de%20Leitura/conteudos/SL_funcoes_organicas.pdf
Texto originalmente publicado em https://www.infoescola.com/quimica-organica/alcenos/