A alanina é um aminoácido proteico não-essencial, dado que é produzida naturalmente pelo organismo humano. Atua como matéria prima para a síntese de glicose no fígado e nos músculos, quando se faz necessário a produção rápida de glicose. No sistema nervoso central (SNC) age como um neurotransmissor inibitório, sendo benéfica para indivíduos epilépticos.
Conteúdo deste artigo
Síntese
No organismo, a alanina tem origem na via metabólica da glicólise, tendo o piruvato e aminoácidos com cadeias laterais ramificadas (valina, leucina e isoleucina, por exemplo) como precursores e, o zinco como cofator. Neste processo, a transferência do grupamento amina, chamada transaminação, para o piruvato resulta na síntese da alanina.
As reações de transaminação são reversíveis e compatíveis com o piruvato, fato que confere facilidade na síntese da alanina, sendo esta relacionada com diversas vias metabólicas, como a glicólise, gliconeogênese e o ciclo do ácido cítrico.
Alanina X Beta-alanina
A diferença entre essas moléculas está na estrutura molecular. Assim, ambas são aminoácidos, mas com estrutura e implicações metabólicas diferentes:
A alanina é transformada em uma molécula fonte de energia aos músculos. Já a beta-alanina, é utilizada para a síntese de carnosina, com função de tampão ao regular a acidez do tecido muscular.
A carnosina é um dipeptídeo, composto pelos aminoácidos beta-alanina e histidina, presente principalmente nos músculos.
Propriedades químicas
A alanina tem como abreviatura Ala ou A. Sua fórmula química é CH3CH(NH2)COOH e apresenta o nome oficial 2-aminopropanóico. No estado puro, é um sólido branco cristalino, inodoro e com sabor adocicado. Trata-se de um aminoácido apolar e estável à temperatura ambiente, sofrendo decomposição a 289ºC (ponto de fusão). Sua massa molar é de 89,09 g/mol e densidade de 1,424g/ml.
No carbono α se encontram ligados os grupamentos amino (-NH2), carboxila (-COOH), um átomo de hidrogênio (H) e a cadeia lateral (grupo R) representado na alanina por um grupo metil, lhe conferindo o caráter apolar e classificando-a como aminoácido alifático. Isto significa que não interage com a água, sendo hidrofóbica e, a cadeia lateral é aberta.
Assim, o carbono α é assimétrico, por possuir quatro ligantes diferentes e, apresenta dois isômeros opticamente ativos, sendo as formas D-alanina e L-alanina. Contudo, a D-alanina está presente apenas na parede celular de determinadas bactérias e em alguns peptídeos antibióticos.
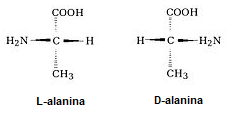
Estrutura química dos isômeros opticamente ativos da Alanina.
Aplicações
A alanina pode ser utilizada como:
- Suplemento alimentar;
- Auxiliar do metabolismo energético e da glicose;
- No SNC, a alanina atua como um neurotransmissor inibitório, com considerada atividade tranquilizante, o que pode auxiliar nos quadros de epilepsia, por reduzir a excitabilidade neuronal.
- Auxiliar na produção de células do sistema imunológico, como os linfócitos e imunoglobulinas.
Ciclo da glicose-alanina
Trata-se de uma via metabólica utilizada por vários tecidos, como o fígado e músculos, para a obtenção contínua da glicose. A alanina desempenha importante função metabólica, onde se observa a degradação de aminoácidos nos tecidos para a obtenção de energia.
No processo, ocorre o transporte dos grupamentos amino para o fígado. Nos músculos, onde há a quebra dos aminoácidos para utilização como fonte de energia, os aminoácidos são capturados sob a forma de glutamato, por transaminação. O glutamato é convertido em glutamina, que é transportada ao fígado, ou sofre ação enzimática. Através da ação da enzima alanina aminotransferase, o glutamato transfere o seu grupo amina para o piruvato, originando a alanina e α-cetoglutarato. A alanina então poderá: transferir seu grupo amina para o α-cetoglutarato, formando glutamato; ser transferida para a corrente sanguínea e transportada para o fígado; no fígado, sofrer reação inversa da enzima alanina aminotransferase, originando piruvato.
O piruvato então dá origem à glicose, através da via da gliconeogênese, que cai na corrente sanguínea e atinge os músculos. Já o glutamato, no fígado, é transportado para as mitocôndrias onde é degradado pela enzima glutamato desidrogenase, originando a amônia, que é tóxica. No ciclo da uréia, a amônia é então convertida em uréia e, posteriormente excretada através da urina.
O fato da gliconeogênese ocorrer no fígado e, não nos músculos, faz com que a energia disponível no músculo possa ser utilizada principalmente para a contração muscular.
Fontes
A alanina é encontrada em diversos alimentos, incluindo: carnes, leite, queijo, castanhas, ovos, aveia, cenoura, milho, ervilhas e berinjela.
Bibliografia:
MARZZOCO, Anita; TORRES, Bayardo Baptista. Bioquímica básica. 3. ed. Rio de Janeiro: Guanabara Koogan, 2007.
Nelson, David L.; COX, Michael M. Princípios de bioquímica de Lehninger. Porto Alegre: Artmed, 2011. 6. ed. Porto Alegre: Artmed, 2014.
Rodrigues, João. Alanina. FC Ciências e tecnologia. Disponível em < https://www.fciencias.com/2013/08/22/alanina-molecula-semana/>.
Texto originalmente publicado em https://www.infoescola.com/bioquimica/alanina/