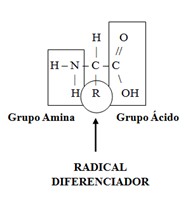
Aminoácidos, ou simplesmente aa, são moléculas orgânicas que apresentam um carbono saturado, denominado de carbono alfa, que realiza uma ligação com um átomo de hidrogênio, com um grupamento amino, com um grupamento ácido e com um radical orgânico qualquer, sendo esta última ligação a que distingue um aminoácido de outro. Com relação à sua denominação, estão presentes as funções amina e ácido carboxílico, obrigatoriamente, em toda molécula de aa. A estrutura elementar de um aa é representada na Figura 1.
Aminoácidos são geralmente compostos de alta polaridade, uma vez que há somente três possibilidades de apresentarem um átomo de carbono alfa que também não seja quiral. Ou seja, um carbono quiral é aquele que se liga quimicamente a quatro grupos distintos. No caso do carbono alfa, apenas quando o radical diferenciador for um átomo de hidrogênio, um grupo amina ou um grupo ácido é que esse carbono alfa não será também quiral.
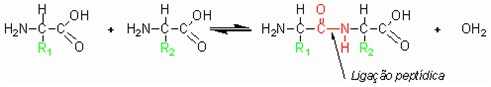
Aminoácidos reagem quimicamente entre si, por meio da representação mostrada na Figura 2.
Conforme pode ser observado, a ligação entre aminoácidos ocorre entre o grupamento carboxílico do primeiro e o grupamento amina do segundo (ou vice-versa), com liberação de uma molécula de água a cada reação formada. O nome dado a essa reação é de ligação peptídica, pois é a reação formadora de um peptídeo.
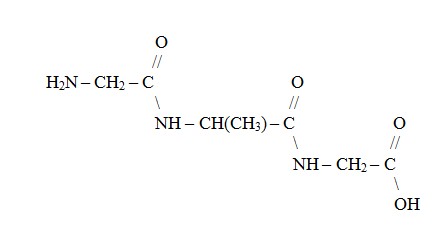
Abaixo, na Figura 3, é mostrado a formação de um peptídeo a partir dos aminoácidos glicina, alanina e glicina.
A molécula formada, denominada de peptídeo, pode ser representada resumidamente por:
H2N – CH2 – CO – NH – CH(CH3) – CO – NH – CH2 – COOH,
ou ainda pelas iniciais dos aminoácidos formadores da mesma,
GLI-ALA-GLI.
As características básicas de uma ligação peptídica (entre dois aminoácidos), resumidamente, são:
- “Origina cadeia (poli)peptídica formada por resíduos de AAs;
- Origina extremidades N-terminal e C-terminal;
- Para que ocorra requer uma complexa maquinaria celular (ribossomos, RNAm, RNAt, enzimas e prots, energia);
- A hidrólise é feita por proteases, ácidos e bases fortes, t°↑;
- Ressonância: apesar de ser representada por 1 único traço, possui características intermediárias entre ligação simples e dupla;
- Átomos que participam da ligação peptídica (H -N -C -O) formam 1 plano rígido;
- A rotação só é possível em torno do Cα”1.
No momento em que se tem muitos aa ligados entre si (o número difere dependendo da fonte adotada, mas gira em torno de 100), deixamos de classificar a molécula formada de peptídeo para então a classificarmos como uma proteína.
Proteínas são polímeros biológicos com elevadas massas molares formadas por unidades fundamentais (monômeros) denominadas aminoácidos. As proteínas são os componentes químicos mais importantes do ponto de vista estrutural, pois estão presente em todas as partes da célula. São também fundamentais no funcionamento do organismo, uma vez que o controle das reações químicas depende das enzimas, que são moléculas de proteínas. “São as moléculas orgânicas mais abundantes e importantes nas células e perfazem 50% ou mais de seu peso seco. São encontradas em todas as partes de todas as células, uma vez que são fundamentais sob todos os aspectos da estrutura e função celulares. Existem muitas espécies diferentes de proteínas, cada uma especializada para uma função biológica diversa. Além disso, a maior parte da informação genética é expressa pelas proteínas. Pertencem à classe dos peptídeos, pois são formadas por aminoácidos ligados entre si por ligações peptídicas. Uma ligação peptídica é a união do grupo amino (-NH2 ) de um aminoácido com o grupo carboxila (-COOH) de outro aminoácido, através da formação de uma amida”².
A lista abaixo apresenta itens que visam a resumir e a elucidar o exposto:
1. A principal diferença entre peptídeos e proteínas.
Um peptídeo pode ser formado pela união de dois aminoácidos e uma proteína só será formada por filamentos de polipeptídios, ou seja, as proteínas são polímeros e os peptídeos são os monômeros.
2. A caracterização de uma reação peptídica.
União do grupo ácido do aminoácido com o grupo amina de outro aminoácido, com liberação de uma molécula de água.
3. Alimentos considerados como fonte de proteína completa.
Um alimento que apresenta todos os 20 aminoácidos necessários para formar as proteínas necessárias para o organismo humano. Alimentos de origem animal, como carne, leite, queijo, peixe e ovos, possuem proteínas de alta qualidade.
4. O que se entende por carbono alfa e quando um carbono alfa será quiral?
Carbono alfa é o carbono em que está ligado a um grupo amina, a um grupo ácido, a um átomo de hidrogênio e a um radical R qualquer. Quando o átomo de carbono está ligado a quatro radicais diferentes, como N2H, COOH, H, R, por exemplo. O único aminoácido que não apresenta composto quiral é a GLICINA, pois apresenta três radicais diferentes (N2H, COOH, H, H), havendo dois radicais hidrogênio.
Referências:
1. http://www.ufpel.edu.br/iqg/db/Apresenta%E7%F5es_PPT
2. http://www.enq.ufsc.br/labs/probio/disc_eng_bioq/trabalhos_pos2003/
FELTRE, Ricardo, Química Orgânica, Ed. Moderna, 6ª Edição, São Paulo, 2004.
LINHARES, Sérgio; GEWANDSZNAJDER, Fernando, Biologia, Ed. Ática, 1ª Edição, São Paulo, 2007.
Texto originalmente publicado em https://www.infoescola.com/bioquimica/aminoacidos-como-formadores-de-peptideos-a-proteinas/