Cromóforos ou grupo cromóforo é a parte ou conjunto de átomos de uma molécula, chamados de grupos funcionais orgânicos que absorvem na região do ultravioleta ou visível. O termo cromóforo também pode ser definido como uma substância que possui muitos elétrons que tem a capacidade de absorver energia ou luz visível. A presença desses grupos funcionais que contém muitos elétrons é responsável pela cor de uma molécula. Ao absorver energia esses elétrons são excitados a um nível energético maior e ao retornarem ao estado fundamental emitem essa radiação, e dependendo do comprimento de onda da energia transmitida, apresentarão uma coloração especifica. A cor que vemos se refere ao comprimento de onda que não é absorvido, ou seja, vemos a cor complementar a cor do comprimento de onda da energia que é absorvida pelos grupos cromóforos. Então se vemos uma cor verde, significa que o cromóforo absorveu energia no comprimento de onda referente a luz vermelha.
Tabela 1. Comprimento de onda das cores e suas complementares
| Comprimento de onda (nm) | Cor absorvida | Cor complementar |
| Abaixo de 380 | Ultravioleta | |
| 380 a 435 | Violeta | Verde-amarelado |
| 435 a 480 | Azul | Amarelo |
| 480 a 490 | Azul-esverdeado | Alaranjado |
| 490 a 500 | Verde-azulado | Vermelho |
| 500 a 560 | Verde | Púrpura |
| 560 a 580 | Verde-amarelado | Violeta |
| 580 a 595 | Amarelo | Azul |
| 595 a 650 | Alaranjado | Azul-esverdeado |
| 650 a 780 | Vermelho | Verde-azulado |
| Acima de 780 | Infravermelho |
Entre os compostos cromóforos temos os que apresentam instaurações (ligações duplas ou triplas), como os alcenos, alcenos conjugados, alcinos, carbonilas, carboxila, amido, azo, nitro, nitroso, nitrato e aromáticos. Como exemplos temos diversos tipos de corantes alimentícios como a tartrazina, pertencente ao grupo funcional dos azo compostos, responsável pela coloração amarela de diversos alimentos.
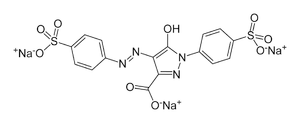
Figura 1. Estrutura da tartrazina.
O β-caroteno também um cromóforo muito comum responsável pela coloração laranja de diversos legumes, como damasco, cenoura, abóbora, podendo ser encontrado também em menor quantidade em folhas de couve, espinafre, brócolis, etc. Essa molécula é precursora da vitamina A.
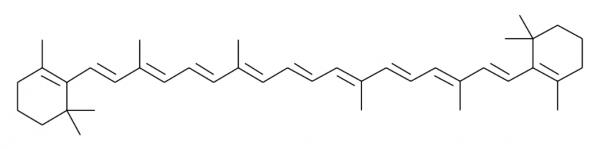
Figura 2. Estrutura do β-caroteno
Entre outros exemplos de cromóforos do tipo temos também os corantes têxteis, licopeno e as antocianinas.
Existem também grupos de cromóforos que se apresentam na forma de complexos metálicos. Entre alguns cromóforos do tipo complexos metálicos mais conhecidos temos a clorofila (que podem ser do tipo a, b, c e d) que consiste de um metal central, o magnésio complexado com ligantes em anel do tipo clorina. Esse complexo é o responsável pela coloração verde das plantas e pelo processo de fotossíntese.
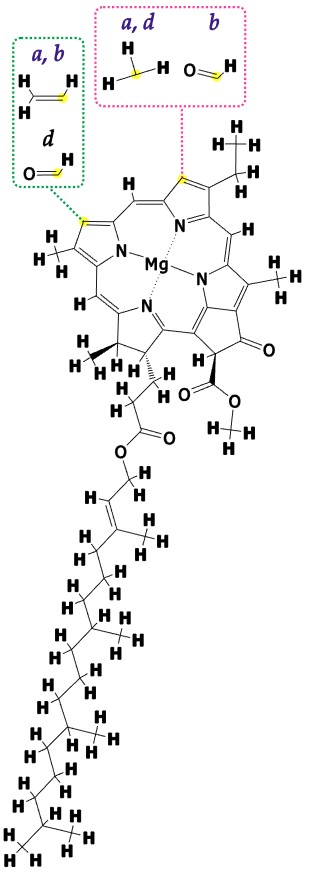
Figura 3. Estrutura comum às clorofilas a, b e d, com os grupos funcionais que as diferenciam em destaque.
Outro cromóforo de bastante importância é a hemoglobina, onde temos um átomo central de ferro complexado a um anel de porfirina. Essa molécula é responsável pela coloração vermelha do sangue e sua função está relacionada com o transporte sanguíneo de oxigênio.
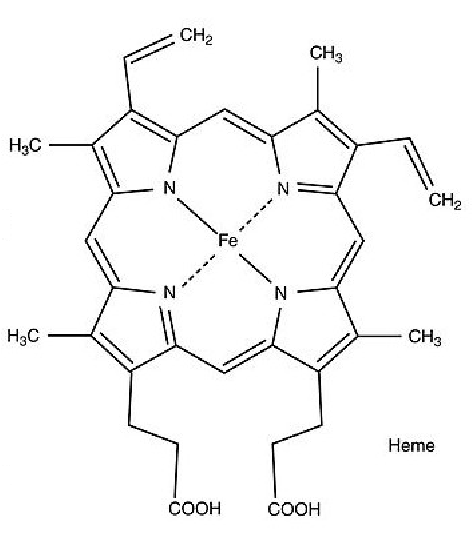
Figura 4. Estrutura da hemoglobina
Outras aplicações dos cromóforos incluem os do tipo auxocromo, que possuem um grupo funcional que modifica a capacidade do cromóforo de absorver luz, ou ainda os halocromos que são substâncias que mudam de cor com a variação do pH. Essa é uma propriedade, por exemplo, dos indicadores que mudam de cor de acordo o pH do meio, como por exemplo a fenolftaleína utilizada em algumas titulações ácido base.
Referencias:
Tito e Canto. Química na Abordagem do Cotidiano. Volume único, parte C – Química Orgânica. Editora Saraiva 2005.
Atkins, P. W.; Jones, Loretta . Princípios de química: questionando a vida moderna e o meio ambiente, volume único. 3. ed. Porto Alegre: Bookman, 2006.
Solomons, T. W. G., Fryhle, C. B. Química Orgânica. Vol 1, 7. ed. Rio de Janeiro, LTC, 2001.
Texto originalmente publicado em https://www.infoescola.com/quimica/cromoforos/